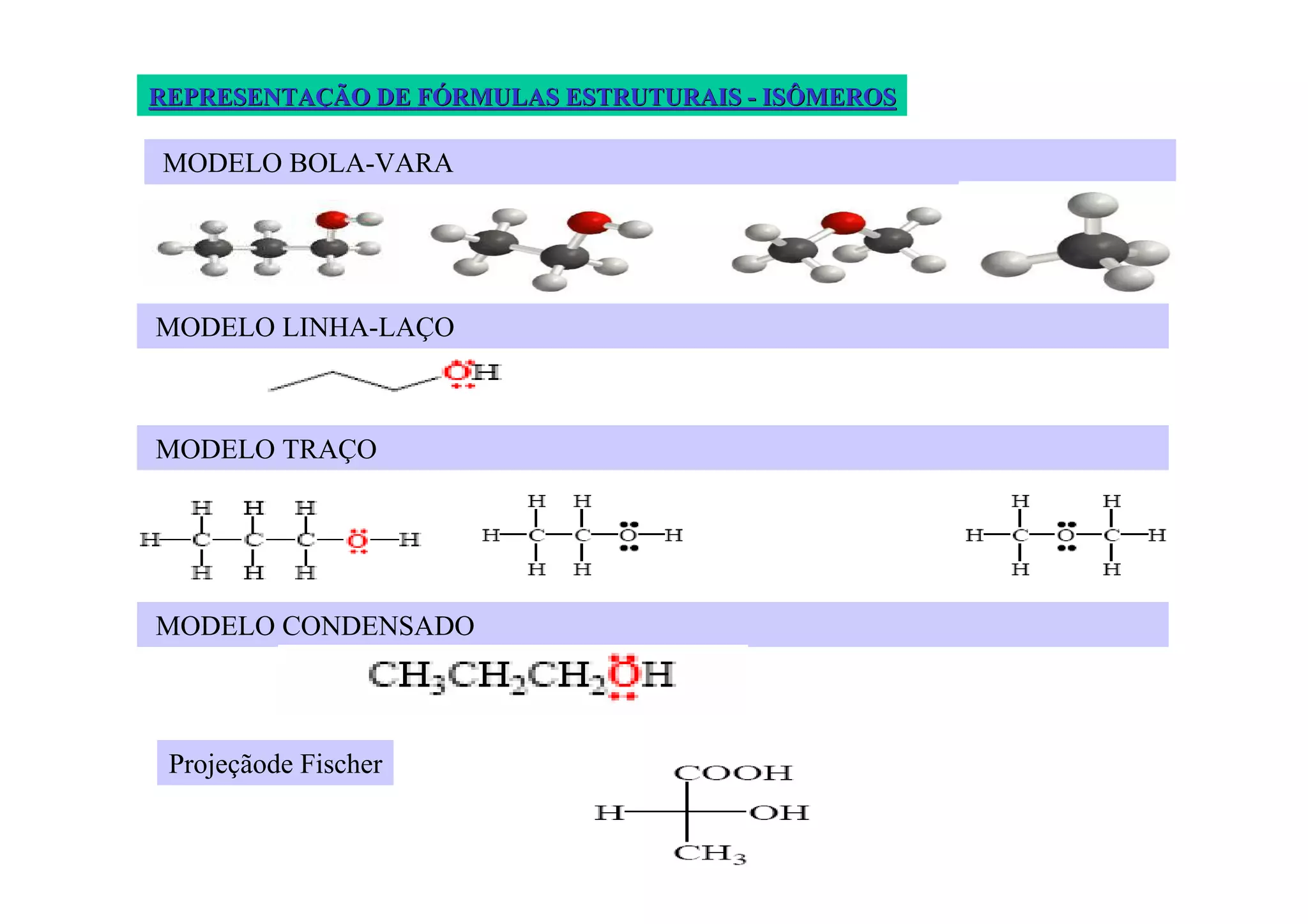
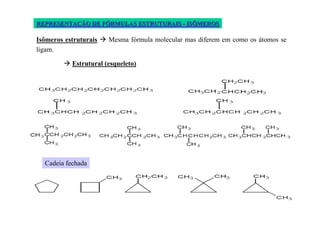
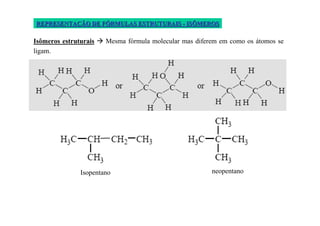
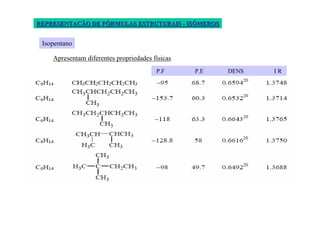
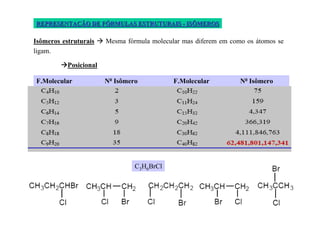
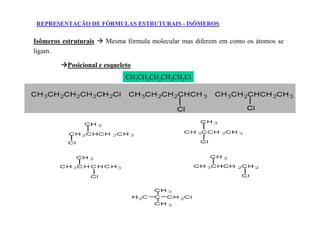
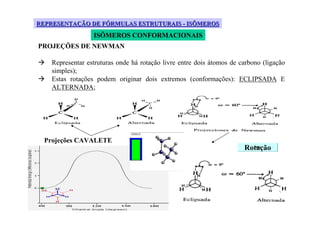
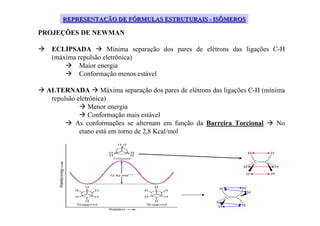
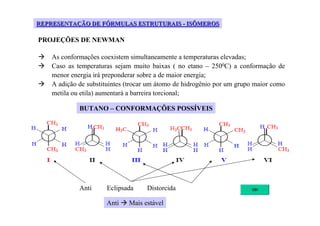
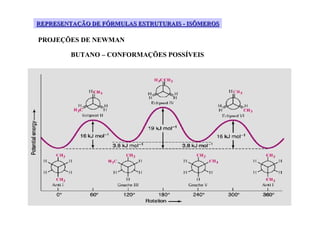
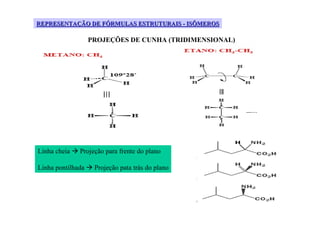
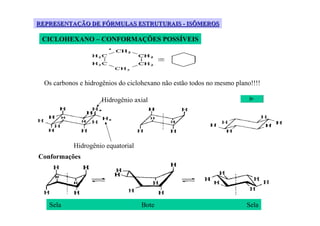
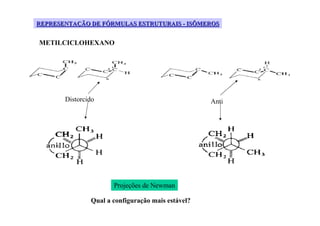
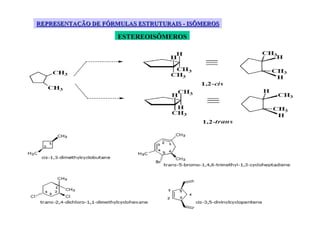
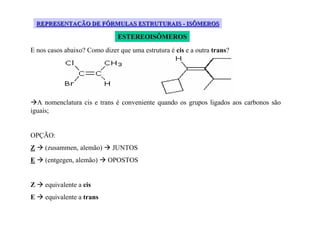
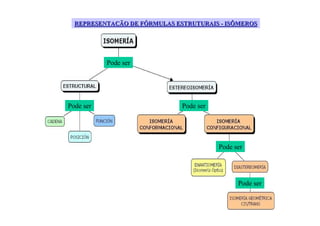
O documento discute diferentes tipos de isômeros, incluindo isômeros estruturais, posicionais e funcionais. Também aborda isômeros conformacionais e estereoisômeros, explicando como a orientação dos átomos no espaço pode levar a propriedades físicas diferentes entre compostos. Finalmente, fornece regras para designar estereoisômeros como cis ou trans.