Incorporar apresentação
Baixado 16 vezes



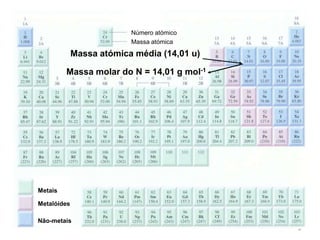

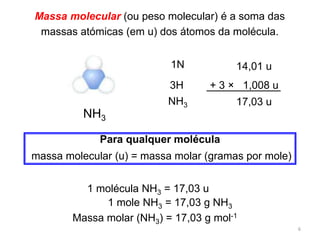
O documento explica os conceitos de mole, massa molar e número de Avogadro. Uma mole contém 6,022x1023 entidades elementares e representa a quantidade de substância contida em exatamente 12 gramas de carbono-12. A massa molar é definida como a massa de 1 mole de uma substância em gramas, e é igual à soma das massas atômicas dos átomos ou moléculas que compõem a substância.





