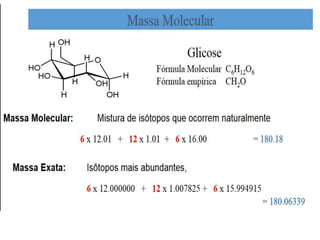
- A unidade de massa atômica (u) equivale a 1/12 da massa de um átomo de carbono-12. A massa atômica representa quanto mais pesado que 1/12 de um átomo de carbono-12 um átomo é.
- As massas atômicas nas tabelas periódicas são médias ponderadas das massas dos isótopos de um elemento.
- O número de Avogadro é o número de átomos em 12,01 gramas de carbono, sendo igual a 6,022 x 1023. Um mol contém este número de part