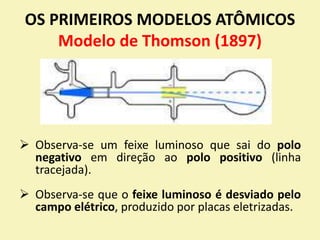
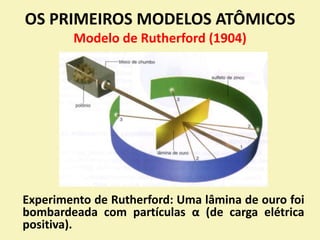
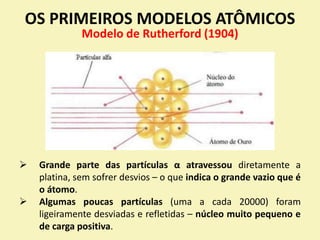
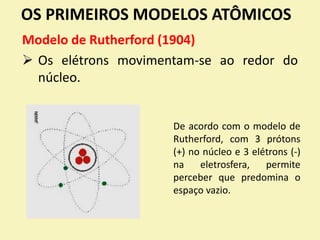
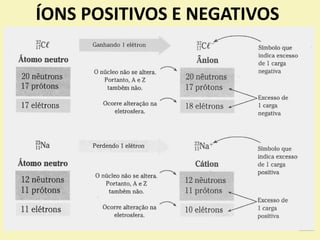
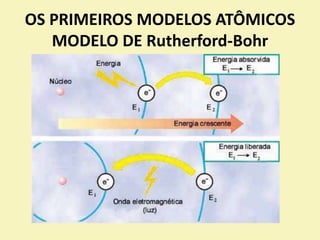
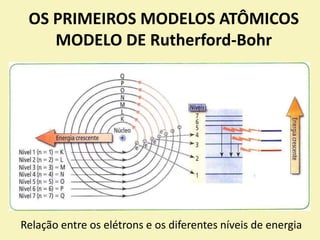
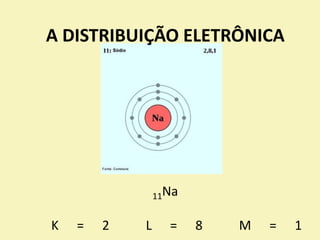
O documento descreve os primeiros modelos atômicos, desde os filósofos gregos até o modelo de Rutherford-Bohr. Inclui os modelos de Dalton, Thomson, Rutherford e o modelo clássico, explicando suas principais características e contribuições para o entendimento da estrutura atômica.