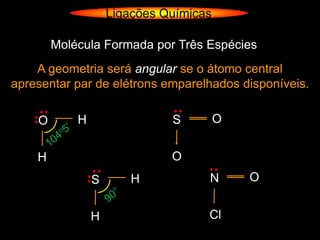
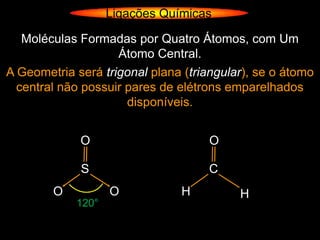
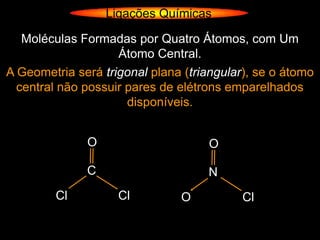
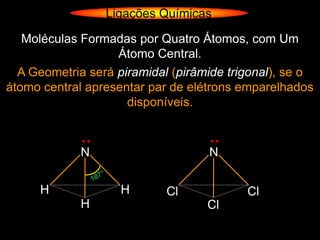
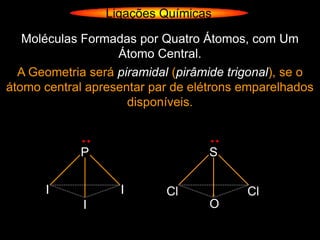
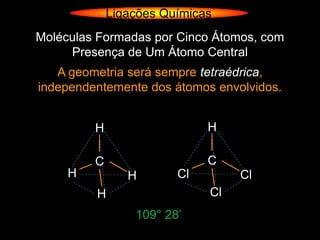
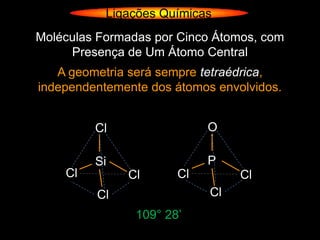
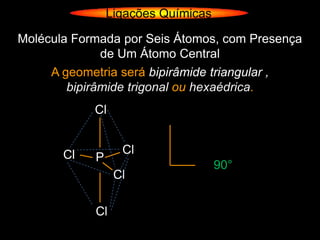
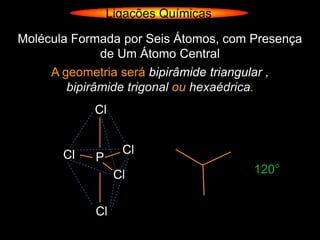
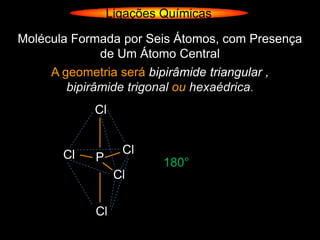
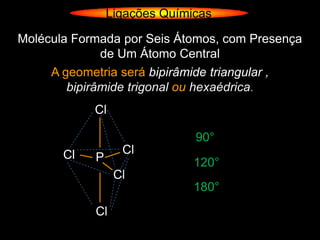
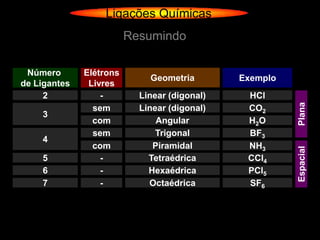
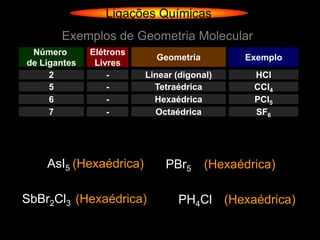
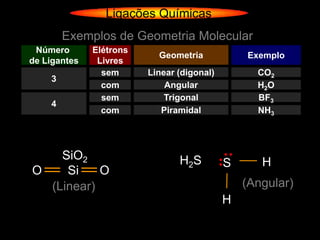
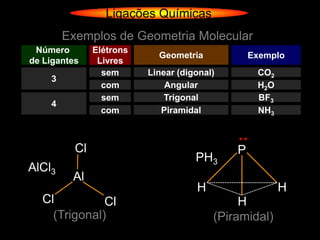
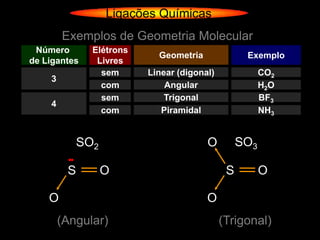
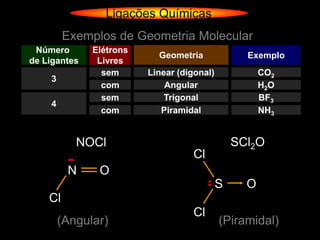
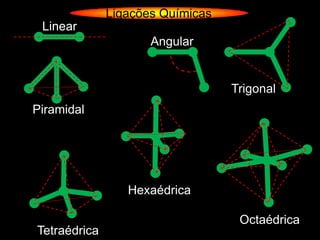
O documento descreve as geometrias moleculares comuns de acordo com o número de átomos ligados e a disponibilidade de elétrons livres no átomo central. Moléculas com 2 átomos ligados geralmente são lineares ou digonais. Moléculas com 3 átomos ligados são lineares ou angulares dependendo da disponibilidade de elétrons livres. Moléculas com 4 ou mais átomos ligados podem ter geometrias como trigonal, piramidal, tetraédrica, hexaédrica ou octaédrica. Exemplos específ