1) O documento apresenta informações sobre espalhabilidade inicial de líquidos, tensão superficial e interfacial e coeficiente de espalhabilidade.
2) São apresentados exemplos de cálculo do coeficiente de espalhabilidade inicial para um produto cosmético oleoso espalhado sobre água.
3) São mostrados dados experimentais sobre adsorção de CO em carvão que serão usados para verificar o modelo de Langmuir e calcular parâmetros.
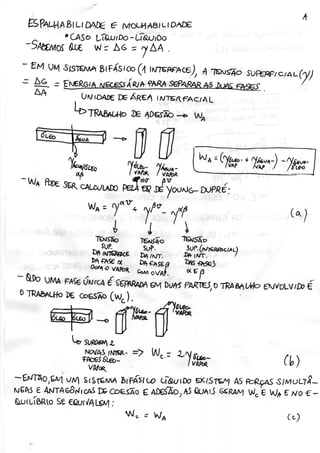

![• CASo L.I<SUJCO-S6UDO
c
'O-
ff;
(1) LTaO|;í»CoMPLeTAMeA/TeeSf/^LM/WX)Í0rO°) -^P(CM€ tf&UlPo
0^0°-* Cos 9 = 1
W
& ri8o -o C05 9 - 1 -o y ^ " - O
^lfz O A Sufeftffaç //Ãò fíR.sc///v L( 24;?
T R A è A L ^ PARA Sé^P/a/V^R o Lr(a,-J/P^
^^1 0< 9 <^S0 : /Vl0LHA8lUDAÍ)£fy^R.cr/HL -t? W A < Wc
I Calcular o coeficiente de cspaihabilidade inicial de um produto cosmético, oleoso, espa-
lhado sobre a água. sabendo que a tensão superficial da água, a 20 "C é 70,2x10*'* N.m"'.
Nesta temperatura, a tensão superficial do produto é 44,4x! 0"^ N.m"^' e sua tensão interfa-
cial frente a água é 1 2 , 0 x 1 0 " ^ N-m"'.
Resposta: Utilizando a Equação 9 . 2 0 e substituindo os respectivos valores, obteremos:
- 1
^inicial
= 7 0 . 2 X 1 0 ^ - ( 4 4 . 4 X 1 0 + I 2 . 0 X 10 ^ ) N T T I ' = 1 3 . 8 X ! 0 " ' ^ N - m
Quando as duas fases líquidas estiverem em contato por tempo suficienie, ocorrerá
troca de matéria entre as mesmas, até se atingir uma concentração de saturação mútua, con-
forme visto no Capítulo 6 - Líquidos imiscíveis.
Considere que nestas condições as tensões superficiais da água, o óleo e a tensão inter-
facial passam a ter os seguintes valores 5 2 , 7xl0~^, 4 9 , I x lO^^c [ 2 , 0 x ] 0 - ^ , respectivamente.'
O coeficiente de cspaihabilidade passa a ser, portanto.
'final = 52.7x10 •'-(49,1x10 + I2.nx 10 " ' i N - m 8.4x10"^ N • m '
O valor positivo inicial de ^ e sua transformação, para um valor negativo indicam que
o líquido se expande inicialmente sobre a superfície da água e se contrai a seguir, deixando
porém uma camada monomolecuJar sobre a fase substrato,](https://image.slidesharecdn.com/isotermasdeadsoro-170516162740/85/Isotermas-de-adsorcao-3-320.jpg)



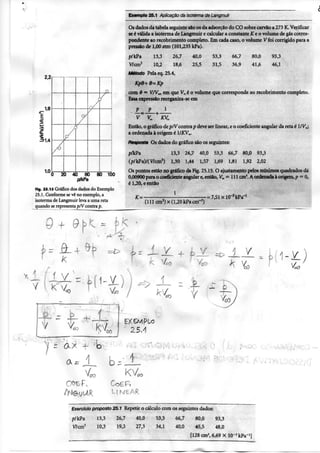
![f-t SA/] TST^eX íçZ>e'55cv^Jp4o.•
r-
b N"-
COMO t>K< 1ff.K, © < ^ G^MPRe/
/](https://image.slidesharecdn.com/isotermasdeadsoro-170516162740/85/Isotermas-de-adsorcao-7-320.jpg)

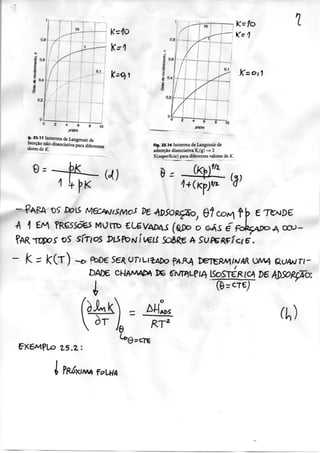


![Exempto 25^ Apiicação da tsoterma BBT
Os dados a seguir são os da adsorção do sobre o rutilo (TioOj) a 75 K. Confirn^a:
que se ajustam à isoterma BET no intervalo de pressão das medidas e detcnri— o s
parâmetros e c.
p/kPa 0,160 1.87 6,11 11.67
V/mra^ 601 720 822 935
17,02
1046
21,92 37.29
125-:
I A 75 K, tcm-se p* = 76,0 kPa. Os volumes foram corrigidos para 1,00 atm e 273 K «
referem-se a 1,00 g de adsorvente.
^^^XÍ^*^ Método A eq. 25.8 pode ser escrita na forau
z 1
••"TF"
Vem entào que (c — l)/cV^^ pode ser estimado pelo coeficiente angular da reta, que
se obtém lançando o primeiro membro da «pressão contra z. O produto cV^^ é dado
pela ordenada à origem da reta mencionada. Os doís resultados combinam-se para
darce V^.
Resposta Coiutrufmos a seguinte tabela:
p/kPa 0.160 1,87 6,11
10^2 2,11 24.6 80.4
10*z/(l -z)(V/mm') 0.035 0,350 1,06
Os pontos dessa tabela estão no gráfico da Fig. 25.20.0 ajustamento pelos mínimo»
quadrados leva à ordenada à origem 0,0589. e então
I
11,67 17,02 21,92 27,29
154 224 288 359
1,95 2,76 3,53 4.47
• = 3,98x 10"^ mm-3
cV
O coeficiente angular da reta é 1,23 X ^0"^ portanto,
c - 1
•=(I.23x 10"^)x lO^x lO-^mm-^Ãj^Sx IQ-^mm"^
As soluções dessas equações são c = 310 e V ^ , = 811 mm'. A 1,00 atm e 273 K, o
volume de 811 ram^ corresponde a 3,6 X 10"^ mol ou 2,2 X 10" átomos. Como cada
átomo ocupa uma área da ordem de 0,16 nm^, a área superficial da amostra é aproxi-
madamente igual a 3,5 m^.
Exercido proposto 2S.3 Repetir o cálculo anterior com os seguintes dados:
p/kPa 0.160 1.87 6.U 11,67 17,02 21,92 27,29
V/cm'' 235 559 649 719 790 860 950
[370,615 cm']
I t
Z. 2
%• f a
1
1
i
1
i
••
/•
j i
i
I i
i >••
1
1 /
1 /
/
< -
i
i /
1 /
- 1 '
•••']
í
_
i
( i
i i
1 i
'Ò 100 200 300 400 500
Itfz
- - _ s í"3 25.20 A isoterma BET é verificada no
tKsjS^^ - gráficodcz/Cl-z)Vcontraz = p/p'.Os
, dadoc sào do Exemplo 25.3.](https://image.slidesharecdn.com/isotermasdeadsoro-170516162740/85/Isotermas-de-adsorcao-13-320.jpg)