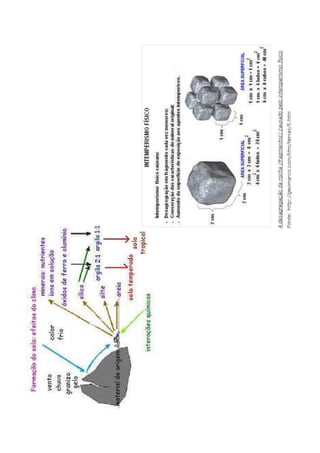
O documento aborda a sedimentação e os processos de intemperismo, erosão, deposição e diagênese que afetam a crosta terrestre. Ele destaca a instabilidade dos minerais das rochas ígneas em condições superficiais e a importância dos silicatos na composição da crosta. Além disso, explica como a decomposição química dos minerais origina novos compostos minerais através de hidratação, oxidação e dissolução.