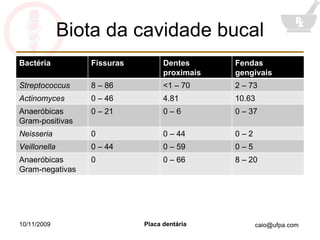
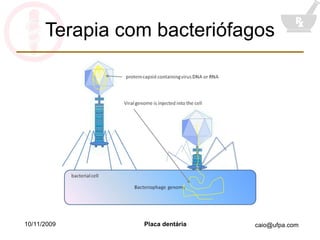
O documento discute a placa dentária bacteriana e biofilmes, incluindo sua formação, composição microbiológica, e relação com doenças como cárie e periodontite. Também aborda agentes antiplaca como clorexidina e flúor, além do potencial uso de bacteriófagos no tratamento da placa.