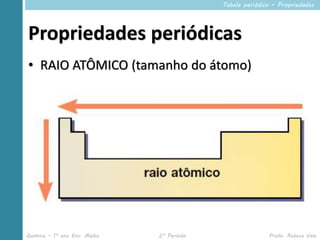
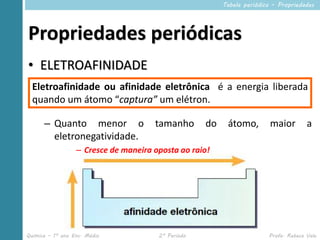
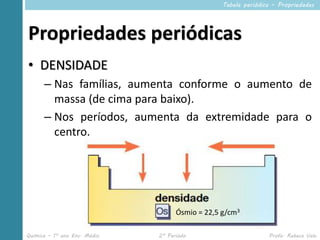
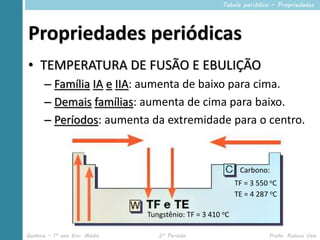
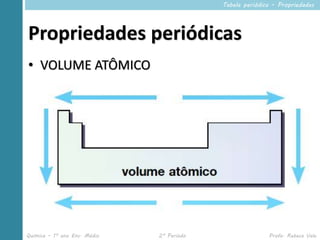
Este documento descreve propriedades periódicas e aperiódicas na tabela periódica. Ele lista propriedades periódicas como raio atômico, energia de ionização e eletronegatividade, explicando como variam periodicamente. Também menciona propriedades aperiódicas como massa atômica que não se repetem periodicamente.