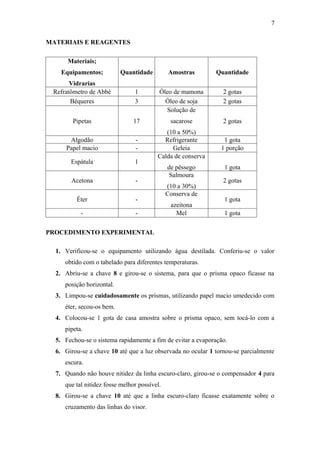
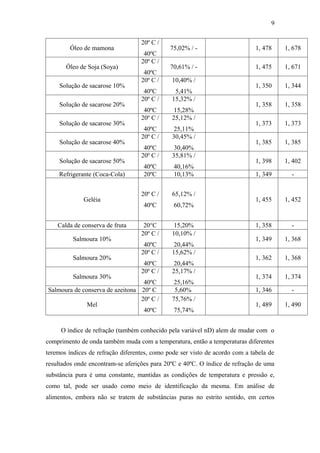
O relatório descreve técnicas de refratometria para determinar o índice de refração e a porcentagem Brix de amostras. Foram medidas amostras de óleos vegetais, soluções de sacarose, alimentos e bebidas usando um refratômetro de Abbé. Os resultados mostraram que o índice de refração e a porcentagem Brix aumentam com a concentração da solução e variam com a temperatura.