1. O documento apresenta uma apostila sobre análise instrumental para um curso técnico em química. 2. A apostila aborda os fundamentos dos principais métodos instrumentais como espectrofotometria, cromatografia e métodos eletroquímicos. 3. O objetivo é fornecer conhecimentos básicos sobre análise instrumental para que os futuros técnicos químicos entendam o funcionamento dos equipamentos.









![Curso: Técnico Químico Análise Instrumental Página: 10
Elaborado por: Profa
Msc. Elaine de Arruda Oliveira Coringa
Leitura amostra original L1 = (Va x Ca) / VT
Leitura amostra+padrão L2 = [(Va x Ca) / VT ] + [ (VP x CP) / VT]
Ca = L1 x CP x VP
(L2 – L1) x Va
1.7 MATEMÁTICA PARA LABORATÓRIO:
1.7.1 Unidades do Sistema Internacional (SI):
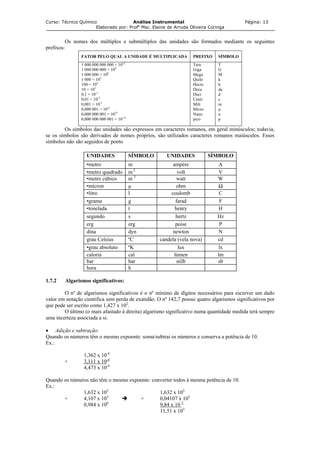
O sistema SI é composto por unidades de medida básicas das quais outras se derivam. Padrões de
comprimento, massa e tempo são o metro (m), o quilograma (Kg) e o segundo (s), respectivamente. A
temperatura é medida em kelvins (K), a quantidade de substancia em mols (mol), a corrente elétrica em
ampére (A).
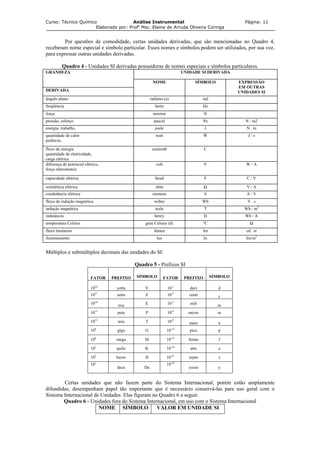
Quadro 2 – Unidades SI de base
[UNIDADES SI DE BASE]
GRANDEZA NOME SÍMBOLO
comprimento metro m
massa quilograma kg
tempo segundo s
corrente elétrica ampère A
temperatura termodinâmica kelvin K
quantidade de matéria mol mol
intensidade luminosa candela cd
As unidades derivadas são unidades que podem ser expressas a partir das unidades de base,
utilizando símbolos matemáticos de multiplicação e de divisão. Dentre essas unidades derivadas, diversas
receberam nome especial e símbolo particular, que podem ser utilizados, por sua vez, com os símbolos de
outras unidades de base ou derivadas para expressar unidades de outras grandezas. O Quadro 3 fornece
alguns exemplos de unidades derivadas expressas diretamente a partir de unidades de base. As unidades
derivadas são obtidas por multiplicação e divisão das unidades de base.
Quadro 3 - Exemplos de unidades SI derivadas, expressas a partir das unidades de base.
[UNIDADE SI]
GRANDEZA
NOME SÍMBOLO
superfície metro quadrado m2
volume metro cúbico m3
velocidade metro por segundo m/s
aceleração metro por segundo ao quadrado m/s2
número de ondas metro elevado à potência
menos um (1 por metro)
m-1
massa específica quilograma por metro cúbico kg/m3
volume específico metro cúbico por quilograma m3
/kg
densidade de corrente ampère por metro quadrado A/m2
campo magnético ampère por metro A/m
concentração
(de quantidade de matéria)
mol por metro cúbico mol/m3
luminância candela por metro quadrado cd/m2
índice de refração (o número) um 1*](https://image.slidesharecdn.com/quimicainstrumental-150806175525-lva1-app6891/85/Quimica-instrumental-10-320.jpg)