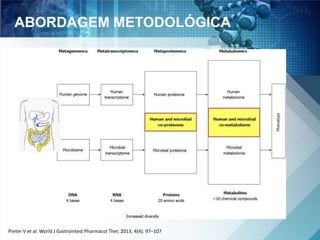
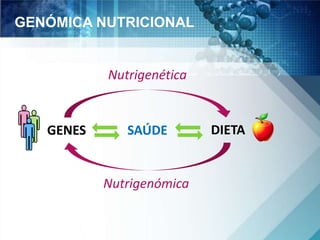
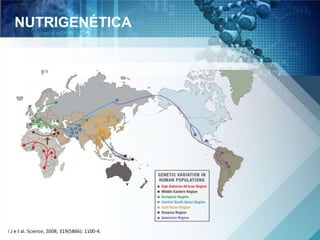
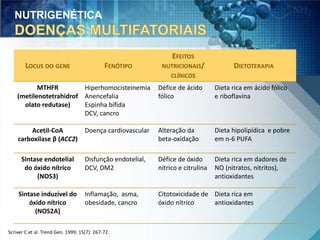
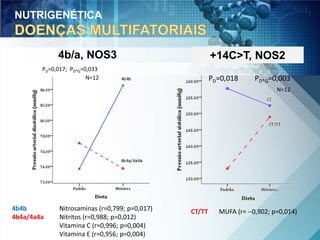
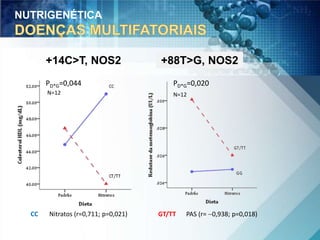
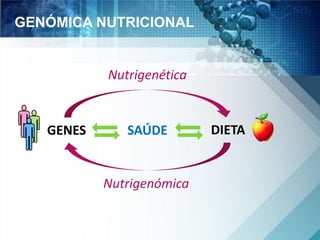
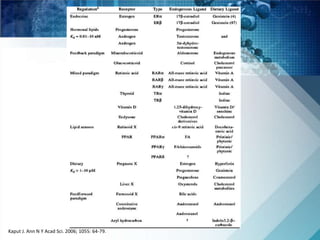
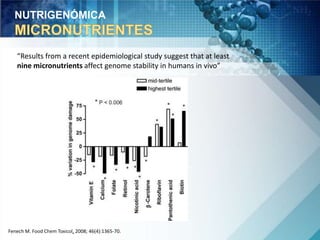
O documento discute a genética nutricional e a nutrigenômica, destacando a importância da personalização da dieta com base no perfil genético individual para a prevenção e tratamento de doenças crônicas. Ele aborda como compostos bioativos dos alimentos interagem com o genoma humano e como as variações genéticas afetam a resposta a dietas específicas. Além disso, menciona a necessidade de estudar fenótipos, biomarcadores e abordagens metodológicas para integrar genômica, proteômica e metabolômica.