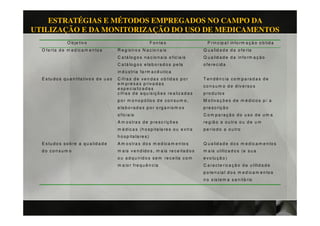
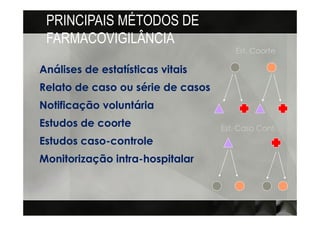
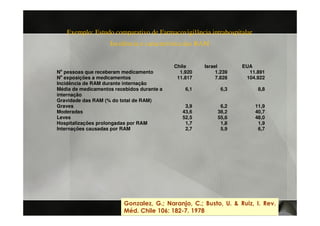
O documento discute conceitos e usos da farmacoepidemiologia. A farmacoepidemiologia estuda o uso e efeitos de medicamentos em populações, focando em efeitos adversos após a comercialização. Ela aplica métodos epidemiológicos para avaliar a utilização e monitorar o uso de medicamentos em nível populacional.