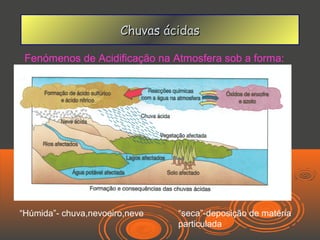
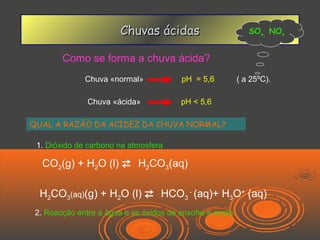
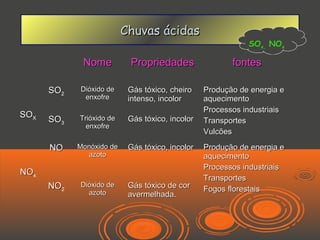
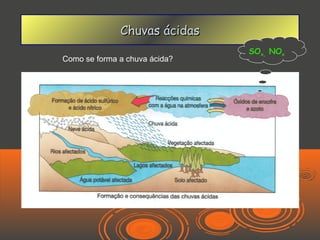
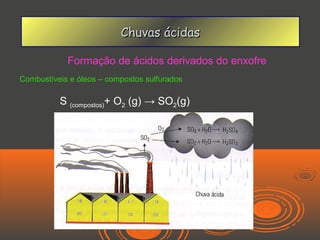
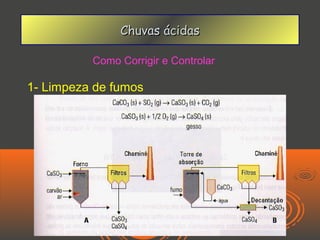
O documento discute chuvas ácidas, explicando que elas são formadas quando óxidos de enxofre e azoto reagem com a água da chuva, tornando-a mais ácida. As principais fontes desses gases poluentes são usinas de energia e veículos a diesel. O documento também discute os efeitos das chuvas ácidas e possíveis medidas para corrigir o problema, como limpeza de fumos e conversores catalíticos.