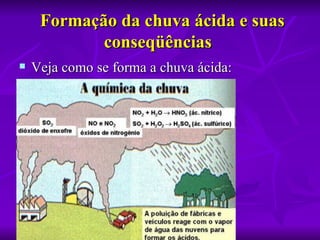
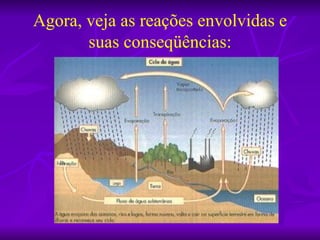
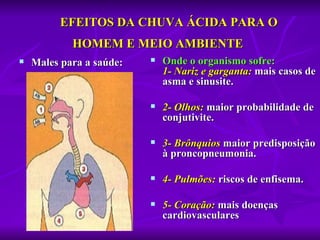
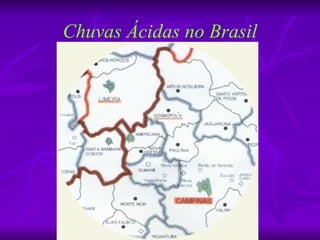
O documento descreve os tipos e causas da chuva ácida, seus efeitos na saúde, meio ambiente e construções, além de formas de evitá-la. A chuva ácida ocorre quando gases como dióxido de enxofre e óxidos de nitrogênio reagem com a água, acidificando-a. Isso pode prejudicar a saúde humana e matar florestas, lagos e edifícios. Reduzir o uso de combustíveis fósseis, adotar transporte público e fontes