O documento fornece informações sobre massa atômica e massa molecular. Em três frases:
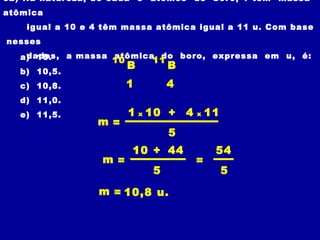
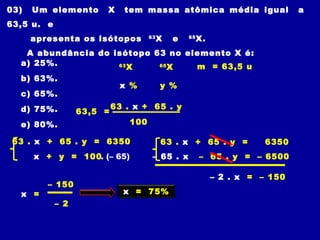
1) A massa atômica indica quantas vezes um átomo é mais pesado que 1/12 do carbono-12 e é usada para calcular a massa molecular.
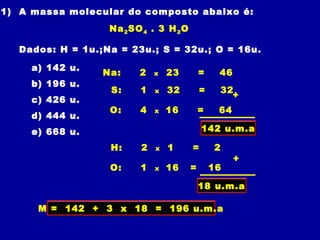
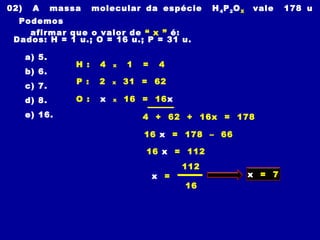
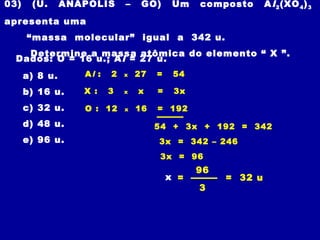
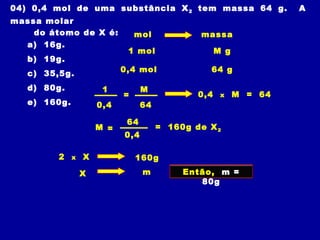
2) A massa molecular soma os pesos atômicos dos átomos de uma molécula e indica quantas vezes uma molécula é mais pesada que 1/12 do carbono-12.
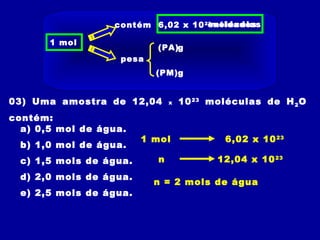
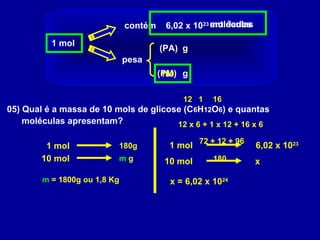
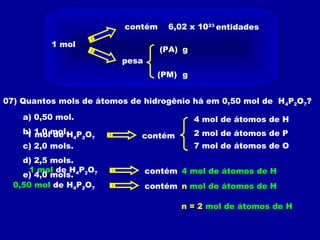
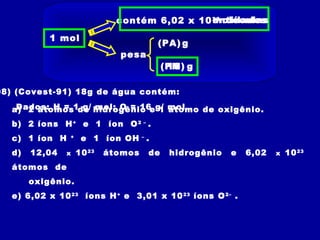
3) O número de Avogadro (6,02 x 1023) relaciona a massa em gra