Atividade de reforço 1° ano
•
0 gostou•2,054 visualizações
Atividades que contemplam os conteúdos estudados nas últimas aulas
Denunciar
Compartilhar
Denunciar
Compartilhar
Baixar para ler offline
Recomendados
AVALIAÇÃO DE CIÊNCIAS - 6º OU 7º ANO - ÁGUA, LIXO, SANEAMENTO BÁSICO E POLUIÇÃO

AVALIAÇÃO DE CIÊNCIAS - 6º OU 7º ANO - ÁGUA, LIXO, SANEAMENTO BÁSICO E POLUIÇÃOSecretaria de Estado de Educação e Qualidade do Ensino
Mais conteúdo relacionado
Mais procurados
AVALIAÇÃO DE CIÊNCIAS - 6º OU 7º ANO - ÁGUA, LIXO, SANEAMENTO BÁSICO E POLUIÇÃO

AVALIAÇÃO DE CIÊNCIAS - 6º OU 7º ANO - ÁGUA, LIXO, SANEAMENTO BÁSICO E POLUIÇÃOSecretaria de Estado de Educação e Qualidade do Ensino
Mais procurados (20)
EXERCÍCIOS DA APOSTILA "MODELOS ATÔMICOS" - 2º ANOS

EXERCÍCIOS DA APOSTILA "MODELOS ATÔMICOS" - 2º ANOS
96513559 7-ano-bacterias-protistas-fungos-virus-com-gabarito cópia

96513559 7-ano-bacterias-protistas-fungos-virus-com-gabarito cópia
Classificação, propriedades e transformações físicas da matéria

Classificação, propriedades e transformações físicas da matéria
Exercicios resolvidos movimento retilíneo uniforme

Exercicios resolvidos movimento retilíneo uniforme
AVALIAÇÃO DE CIÊNCIAS - 6º OU 7º ANO - ÁGUA, LIXO, SANEAMENTO BÁSICO E POLUIÇÃO

AVALIAÇÃO DE CIÊNCIAS - 6º OU 7º ANO - ÁGUA, LIXO, SANEAMENTO BÁSICO E POLUIÇÃO
Semelhante a Atividade de reforço 1° ano
Semelhante a Atividade de reforço 1° ano (20)
"Somos Físicos" Balanceamento das Equações Químicas

"Somos Físicos" Balanceamento das Equações Químicas
E s t e q u i o m e t r i a relação de massa em solução

E s t e q u i o m e t r i a relação de massa em solução
Exercícios resolvidos de Microfísica da Precipitação

Exercícios resolvidos de Microfísica da Precipitação
Mais de Escola Pública/Particular
Mais de Escola Pública/Particular (20)
Último
Último (20)
Dicionário de Genealogia, autor Gilber Rubim Rangel

Dicionário de Genealogia, autor Gilber Rubim Rangel
PROJETO DE EXTENSÃO - EDUCAÇÃO FÍSICA BACHARELADO.pdf

PROJETO DE EXTENSÃO - EDUCAÇÃO FÍSICA BACHARELADO.pdf
PRÉDIOS HISTÓRICOS DE ASSARÉ Prof. Francisco Leite.pdf

PRÉDIOS HISTÓRICOS DE ASSARÉ Prof. Francisco Leite.pdf
Considere a seguinte situação fictícia: Durante uma reunião de equipe em uma...

Considere a seguinte situação fictícia: Durante uma reunião de equipe em uma...
Projeto de Extensão - ENGENHARIA DE SOFTWARE - BACHARELADO.pdf

Projeto de Extensão - ENGENHARIA DE SOFTWARE - BACHARELADO.pdf
planejamento_estrategico_-_gestao_2021-2024_16015654.pdf

planejamento_estrategico_-_gestao_2021-2024_16015654.pdf
Slides Lição 05, Central Gospel, A Grande Tribulação, 1Tr24.pptx

Slides Lição 05, Central Gospel, A Grande Tribulação, 1Tr24.pptx
ATIVIDADE - CHARGE.pptxDFGHJKLÇ~ÇLJHUFTDRSEDFGJHKLÇ

ATIVIDADE - CHARGE.pptxDFGHJKLÇ~ÇLJHUFTDRSEDFGJHKLÇ
PROVA - ESTUDO CONTEMPORÂNEO E TRANSVERSAL: LEITURA DE IMAGENS, GRÁFICOS E MA...

PROVA - ESTUDO CONTEMPORÂNEO E TRANSVERSAL: LEITURA DE IMAGENS, GRÁFICOS E MA...
PROVA - ESTUDO CONTEMPORÂNEO E TRANSVERSAL: LEITURA DE IMAGENS, GRÁFICOS E MA...

PROVA - ESTUDO CONTEMPORÂNEO E TRANSVERSAL: LEITURA DE IMAGENS, GRÁFICOS E MA...
Atividade de reforço 1° ano
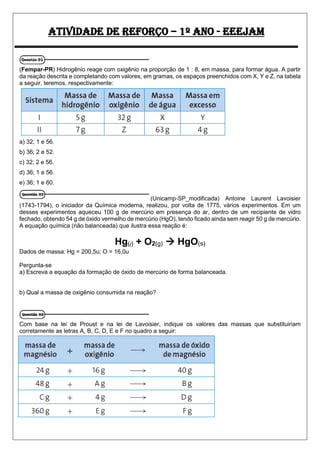
- 1. ATIVIDADE DE REFORÇO – 1º ANO - EEEJAM (Fempar-PR) Hidrogênio reage com oxigênio na proporção de 1 : 8, em massa, para formar água. A partir da reação descrita e completando com valores, em gramas, os espaços preenchidos com X, Y e Z, na tabela a seguir, teremos, respectivamente: a) 32; 1 e 56. b) 36; 2 e 52. c) 32; 2 e 56. d) 36; 1 e 56. e) 36; 1 e 60. (Unicamp-SP_modificada) Antoine Laurent Lavoisier (1743-1794), o iniciador da Química moderna, realizou, por volta de 1775, vários experimentos. Em um desses experimentos aqueceu 100 g de mercúrio em presença do ar, dentro de um recipiente de vidro fechado, obtendo 54 g de óxido vermelho de mercúrio (HgO), tendo ficado ainda sem reagir 50 g de mercúrio. A equação química (não balanceada) que ilustra essa reação é: Hg(l) + O2(g) HgO(s) Dados de massa: Hg = 200,5u; O = 16,0u Pergunta-se a) Escreva a equação da formação de óxido de mercúrio de forma balanceada. b) Qual a massa de oxigênio consumida na reação? Com base na lei de Proust e na lei de Lavoisier, indique os valores das massas que substituiriam corretamente as letras A, B, C, D, E e F no quadro a seguir:
- 2. (UFMG) A tabela indica algumas das massas, em gramas, das espécies envolvidas em dois experimentos diferentes segundo a reação genérica A + B C + 2D. Outras massas estão indicadas pelas letras x, y, w e z. Calcule estas. Dada a reação de combustão do álcool etílico, encontre os valores das massas que substituiriam corretamente as letras de A até L no quadro a seguir, com base nas leis ponderais. (FCMSC-SP) A frase: “Do nada, nada; em nada, nada pode transformar-se” relaciona-se com as ideias de: a) Dalton. b) Proust. c) Boyle. d) Lavoisier. e) Gay-Lussac. Ao se passar uma corrente contínua na água (eletrólise), ela é decomposta em seus constituintes: hidrogênio e oxigênio. Os dados experimentais mostram que as massas dessas duas substâncias sempre estarão na mesma proporção de 1:8, seguindo a Lei Ponderal de Proust. Essas reações também seguem a lei de Lavoisier, isto é, a massa no sistema permanece constante. Com base nessas leis, indique a alternativa que traz os respectivos valores das massas (em gramas) que substituiriam corretamente as letras A, B, C e D nesses experimentos: Massa da Massa do Massa do Água hidrogênio oxigênio 1º experimento A 0,5 g 4,0 g 2º experimento 9,0 g B 8,0 g 3º experimento 18,0 g 2,0 g C 4º experimento D 11,11 g 88,88 g a) 4,5/ 1,0/ 16,0/ 99,99. b) 3,5/ 0,1/ 20,0/ 8,0. c) 5,0/ 17,0/ 28,0/ 8,8. d) 6,0/2,0/ 16,0/ 8,0. e) 4,5 1,0/ 20,0/8,8.
