Soluções
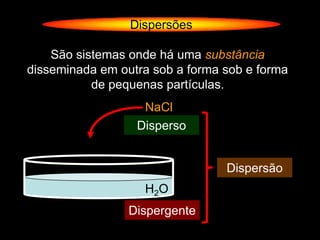
- 1. Dispersões São sistemas onde há uma substância disseminada em outra sob a forma sob e forma de pequenas partículas. NaCl Disperso Dispersão H2O Dispergente
- 2. Dispersões São sistemas onde há uma substância disseminada em outra sob a forma sob e forma de pequenas partículas. H2O
- 3. Dispersões São sistemas onde há uma substância disseminada em outra sob a forma sob e forma de pequenas partículas. Dispersão H2O
- 4. Dispersões Classificação das Dispersões São misturas homogêneas de Soluções Verdadeiras duas ou mais substâncias. São misturas homogêneas (nível macroscópico) ou Soluções Coloidais heterogêneas (nível microscópico) de duas ou mais substâncias. São misturas heterogêneas Suspensões de duas ou mais substâncias.
- 5. Dispersões Classificação das Dispersões NaCl + H2O Solução Verdadeira
- 6. Dispersões Classificação das Dispersões GELATINA Solução Coloidal
- 7. Dispersões Classificação das Dispersões SiO2 + H2O Suspensão
- 8. Dispersões Classificação das Dispersões MAIONESE Solução Coloidal
- 9. Dispersões Classificação das Dispersões C6H12O6 + H2O Solução Verdadeira
- 10. Dispersões Classificação das Dispersões FULIGEM Suspensão
- 11. Dispersões Classificação das Dispersões Soluções Soluções Suspensões Verdadeiras Coloidais 0 – 1 nm 1 – 1000 nm < 1000 nm
- 12. Dispersões São sistemas onde há uma substância disseminada em outra sob a forma sob e forma de pequenas partículas. NaCl Disperso Dispersão H2O Dispergente
- 13. Soluções Verdadeiras São misturas homogêneas (em qualquer nível) de duas ou mais substâncias. NaCl Soluto (ST) Disperso Solução (SL) Dispersão H2O Solvente (SV) Dispergente
- 14. Soluções Classificação das Soluções Quanto ao Estado de Agregação da Solução Sólidas Ouro 18 K (75% Au e 25% Outros) Líquidas Sal em Água Gasosas Ar (80% N2 e 20% O2)
- 15. Soluções Classificação das Soluções Quanto ao Estado de Agregação ST/SV Sólido - Sólido Liga de CuNi Sólido - Líquido Sal em Água Sólido - Gás Naftalina no Ar Líquido - Sólido Água em Amido Líquido - Líquido Água em Álcool
- 16. Soluções Classificação das Soluções Quanto ao Estado de Agregação ST/SV Líquido - Gás Umidade do Ar Gás - Sólido H2 em Pt Gás - Líquido CO2 em Bebidas Gás - Gás CO2 no Ar
- 17. Soluções Classificação das Soluções Quanto a Proporção ST/SV Diluídas Pouco ST e Muito SV Concentradas Muito ST e Pouco SV
- 18. Soluções Classificação das Soluções Quanto a Natureza do Soluto Moleculares C6H12O6 em Água Iônicas NaCl em Água
- 19. Soluções Regra de Solubilidade “Semelhante dissolve semelhante” DISSOLVE Polar Polar DISSOLVE Apolar Apolar DISSOLVE Inorgânico Inorgânico DISSOLVE Orgânico Orgânico
- 20. Soluções Coeficiente de Solubilidade: (CS) É a máxima quantidade de soluto que pode ser dissolvida por um solvente em uma solução. CSNaCl= 36g de NaCl / 100g de H2O 36g NaCl 100g de H2O
- 21. Soluções Coeficiente de Solubilidade: (CS) QST < CS SL Não Saturada ou Insaturada QST = CS SL Saturada QST > CS SL Saturada com PPT QST > CS SL Supersaturada (Solúvel)
- 22. Soluções Coeficiente de Solubilidade: (CS) Coeficiente de Solubilidade g de soluto / 100g de água (Saturada com PPT ou Supersaturada) (Saturada) (Insaturada) Temperatura (°C)
- 23. Soluções Coeficiente de Solubilidade: (CS) Coeficiente de Solubilidade g de soluto / 100g de água (Soluções Gasosas) Temperatura (°C)
- 24. Soluções Coeficiente de Solubilidade: (CS) Endotérmicos Coeficiente de Solubilidade g de soluto / 100g de água Exotérmicos Temperatura (°C)
- 25. Soluções Coeficiente de Solubilidade: (CS) CS (g ST / 100g H2O) Temperatura (°C) 30 20 35 40 X :∆ 50 :∆ - 40 - 60 45 80 X – 40 50 – 60 = ∴ X = 37,5 5 20
- 26. Soluções Unidades de Concentrações: (UC) Quantidade de Soluto UC = Quantidade de Solvente ou Solução
- 27. Soluções Unidades de Concentrações: (UC) Concentração Comum: (C) mST C= (g / L) VSL
- 28. Soluções Unidades de Concentrações: (UC) Concentração Molar: (M) nST M= (mol/L) Como: n = m/MM VSL mST M= (mol/L) MMST .VSL
- 29. Soluções Unidades de Concentrações: (UC) Densidade: (d) mST mSV dST = (g/cm3) dSV = (g/cm3) VST VSV mSL dSL = (g/cm3) VSL
- 30. Soluções Unidades de Concentrações: (UC) Títulos: (τ) Em Massa: (τM) Em Volume: (τV) mST VST τM = (Admensional) τV = (Admensional) mSL VSL 0<τ<1 Percentual: (τ%) τ% = 100 . τ % 0% < τ% < 100%
- 31. Soluções Unidades de Concentrações: (UC) Títulos: (τ) Em PPM Massa: (τPPMM) Em PPM Volume: (τPPMV) mST VST τPPMM = (mg/Kg) τPPMV = (mL/M3) mSL VSL Em PPM Massa/Volume: (τPPMM/V) mST τPPMM/V = (mg/L) VSL
- 32. Soluções Unidades de Concentrações: (UC) Fração Molar: (X) nST nSV XST = (adm.) XSV = (adm.) nSL nSL XSL = 1 (adm.)
- 33. Soluções Unidades de Concentrações: (UC) Molalidade: (W) nST W= (mol/kg) mSV
- 34. Soluções Relações entre as Unidades de Concentrações C = 1000 . τ . d M = C / molST M = 1000 . τ . d / molST τ = τPPM . 10-6 τ% = τPPM . 10-4 % C = τPPM . 10-3 .d M = τPPM . 10-3 .d / molST
- 35. Soluções Processos Diluição: Conc.↓ (1g sal) (1g sal) + 500mL H2O 1L de H2O 1,5L de H2O (1) (2) m1 = m2 C1.V1 = C2.V2 V2 = V1 + Vágua
- 36. Soluções Processos Evaporação: Conc.↑ (1g sal) (1g sal) – 500mL H2O 2L de H2O 1,5L de H2O (1) ∆ (2) m1 = m2 C1.V1 = C2.V2 V2 = V1 – Vágua
- 37. Soluções Processos Mistura de Soluções Solutos Iguais (1g sal) (3g sal) m3 = m1 + m2 1L de H2O 1,5L de H2O C3.V3 = C1.V1 + C2.V2 (1) (2) (4g sal) V3 = V1 + V2 2,5L de H2O (3)
- 38. Soluções Processos Mistura de Soluções Solutos Iguais Cn+1.Vn+1=C1.V1+C2.V2+...+CnVn (1g sal) (3g sal) 1L de H2O 1,5L de H2O Vn+1=V1+V2+...+Vn (1) (2) Para “n” Soluções (4g sal) 2,5L de H2O (3)
- 39. Soluções Processos Mistura de Soluções Solutos Diferentes Sem Reação (1g sal) (3g sal) Sal 1 m1 = m1,3 C1.V1 = C1,3. V3 (1L de H2O) (1,5L de H2O) Sal 2 (1) (2) m2 = m2,3 C2.V2 = C2,3. V3 1g Sal (2,5L(3) H2O) 3g Sal de V3 = V1 + V2
- 40. Soluções Processos Mistura de Soluções Solutos Diferentes Sem Reação KCl KCl 200mL 0,3M M1.V1 = M1,3. V3 0,3.200 = M1,3. 500 M1,3 = 0,12M NaBr NaBr 300mL 0,1M M2.V2 = M2,3. V3 0,1.300 = M2,3. 500 M2,3 = 0,06M Mtotal = 0,12 + 0,06 = 0,18M
- 41. Soluções Processos Mistura de Soluções Solutos Diferentes Sem Reação KCl M3.V3 = M1.V1 + M2.V2 200mL 0,3M M3 . 500 = 0,3. 200 + 0,1. 300 NaBr 300mL 0,1M M3 = 0,18M Mtotal = 0,12 + 0,06 = 0,18M
- 42. Soluções Processos Mistura de Soluções Solutos Diferentes Com Reação Cálculo Estequiométrico
- 43. Soluções Processos Titulação (Padrão) (Problema) (Padrão) HCl KOH 200mL 0,3M 300mL ? (Problema) + (Fenolftaleína)
- 44. Soluções Processos Titulação (Padrão) (Problema) (Padrão) HCl KOH 200mL 0,3M 300mL 0,2M ? (Problema) + (Fenolftaleína) Qác = Qba nác.Xác = nba.Xba Mác.Vác. Xác = Mba.Vba. Xba 0,3. 200.1 = Mba. 300. 1 Mba. = 0,2 M
- 45. Soluções Processos Titulação (Padrão) (Problema) (Padrão) H4P2O7 Fe(OH)3 20mL 0,4M 15mL ? (Problema) + (Fenolftaleína)
- 46. Soluções Processos Titulação (Padrão) (Problema) (Padrão) H4P2O7 Fe(OH)3 20mL 0,4M 15mL 0,71M ? (Problema) + (Fenolftaleína) Qác = Qba nác.Xác = nba.Xba Mác.Vác. Xác = Mba.Vba. Xba 0,4. 20. 4 = Mba. 15. 3 Mba. = 0,71 M
- 47. Soluções Processos Titulação (Padrão) (Problema) H2S Ag2CO3 ? 0,3M 27,6g Qác = Qsa nác.Xác = nsa.Xsa Mác.Vác. Xác = msa/MMsa. Xsa 0,3. Vác. 2 = 27,6/ 276. 2 Vác. = 0,33 L
