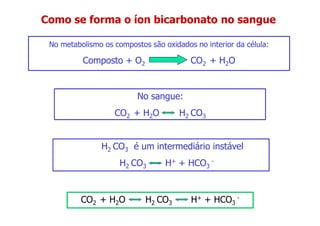
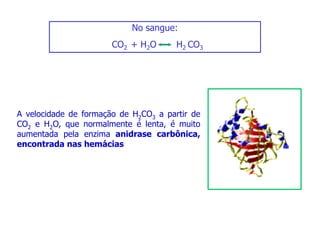
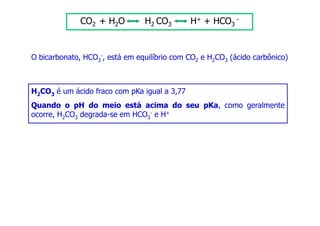
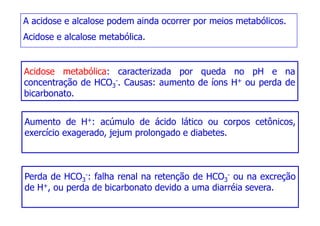
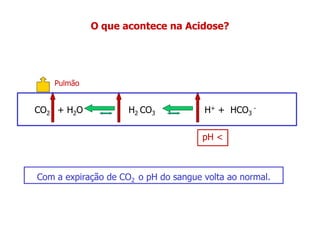
O documento descreve os sistemas tampão no organismo, especificamente: (1) O íon bicarbonato é o principal responsável pelo tamponamento do sangue humano; (2) Ele se forma a partir da reação do dióxido de carbono com a água no sangue; (3) Os principais tampões biológicos mantêm o pH sanguíneo entre 7,35-7,45, resistindo a variações ácidas ou alcalinas.
![Equação de Henderson-Hasselbach
Equação de Henderson-Hasselbach
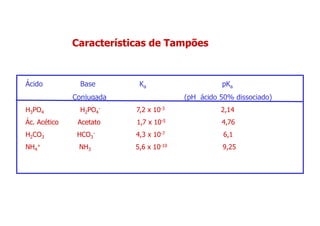
relaciona a Keq (Ka) e as [Ácido] e [Base conjugada]
pH = pKa + log [A-]
[HA]](https://image.slidesharecdn.com/tampoesbiologicos-230225033347-06607352/85/tampoes_biologicos-pdf-3-320.jpg)
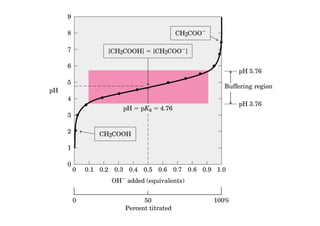
![A eficiência de um tampão está restrita a
uma faixa de pH
pH = pK + log [A-] pH = pK + log [base conjugada]
pH = pKa + log [A-]
[HA]
pH = pKa + log [base conjugada]
[ácido conjugado]
pKa = pH que provoca 50% de dissociação do ácido
[HA] = [A-]
A eficiência máxima de um tampão é no pH
correspondente a seu pKa
Depende também da concentração das espécies](https://image.slidesharecdn.com/tampoesbiologicos-230225033347-06607352/85/tampoes_biologicos-pdf-4-320.jpg)