1. O documento descreve procedimentos para determinar a densidade de amostras sólidas e líquidas.
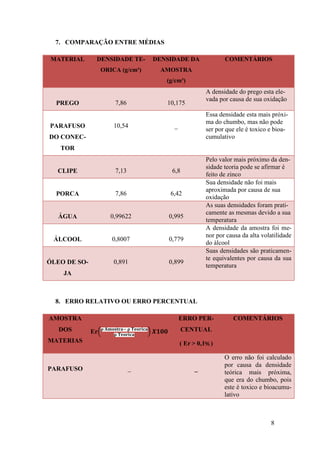
2. Foram medidas as densidades de vários materiais como pregos, parafusos, clipes, água, álcool e óleo.
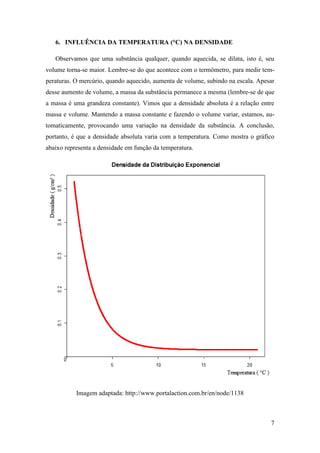
3. A densidade pode ser afetada por fatores como temperatura e composição do material.