A velocidade de uma reação química depende de fatores como a temperatura, concentração dos reagentes e natureza dos reagentes envolvidos. O documento apresenta questões sobre cinética química que abordam esses fatores e conceitos como velocidade média de reação, ordem de reação e fatores que afetam a colisão molecular.
![VELOCIDADE DE UMA REAÇÃO
01) (UFV-MG) Assinale o fenômeno que apresenta velocidade média maior.
a) A combustão de um palito de fósforo.
b) A transformação de rochas em solos.
c) A corrosão de um automóvel.
d) O crescimento de um ser humano.
e) A formação do petróleo a partir de seres vivos.
02) (Fuvest-SP) O seguinte gráfico refere-se ao estudo cinético de uma reação química.
velocidade
da reação
temperaturaT1
O exame desse gráfico sugere que, à temperatura T1, a reação em questão é:
a) lenta.
b) explosiva.
c) reversível.
d) endotérmica.
e) de oxidoredução.
03) A revelação de uma imagem fotográfica em um filme é um processo controlado pela cinética química da
redução do halogeneto de prata por um revelador. A tabela abaixo mostra o tempo de revelação de um
determinado filme, usando um revelador D-76.
nº de mols do revelador tempo de revelação (min)
24 6
22 7
21 8
20 9
18 10
A velocidade média (vm) de revelação, no intervalo de tempo de 7 min a 10 min, é:
a) 3,14 mols de revelador / min.
b) 2,62 mols de revelador / min.
c) 1,80 mols de revelador / min.
d) 1,33 mols de revelador / min.
e) 0,70 mol de revelador / min.
04) A relação a seguir mostra a variação da concentração de uma substância A, em função do tempo, em
uma reação química: a A + b B c C + d D
T(min) 0,0 2,0 4,0 6,0 8,0 10,0 12,0 14,0 16,0 18,0
[A] 11,0 7,0 4,3 3,0 2,0 1,0 0,5 0,3 0,2 0,2
Qual será o valor da velocidade média da reação de A correspondente ao intervalo entre 4 e 14 min?
a) 4,0 mol/L.min.
b) 0,4 mol/L.min.
c) 1,4 mol/L.min.
d) 25 mol/L.min.
e) 2,5 mol/L.min.
1](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/75/Cineticaquimica-1-2048.jpg)
![05) Seja a reação: X Y + Z. A variação na concentração de X em função do tempo é:
X (mol/L) 1,0 0,7 0,4 0,3
tempo(s) 0 120 300 540
A velocidade média da reação no intervalo de 2 a 5 minutos é:
a) 0,3 mol/L.min.
b) 0,1 mol/L.min.
c) 0,5 mol/L.min.
d) 1,0 mol/L.min.
e) 1,5 mol/L.min.
06) (Covest-2006) A reação de decomposição da amônia gasosa foi realizada em um recipiente fechado:
2 NH3 → N2 + 3 H2
A tabela abaixo indica a variação na concentração de reagente em função do tempo.
Concentração de NH3 em mol L
-1
8,0 6,0 4,0 1,0
Tempo em horas 0 1,0 2,0 3,0
Qual é a velocidade média de consumo do reagente nas duas primeiras horas de reação?
a) 4,0 mol L-1
h-1
b) 2,0 mol L-1
h-1
c) 10 km h-1
d) 1,0 mol L-1
h-1
e) 2,3 mol h-1
07) (Mack-SP) Na reação a seguir: X + 2 Y Z, observou-se a variação da concentração de X em função
do tempo, segundo a tabela abaixo:
Tempo (s) 0 120 240 360 720
[X] mol/L 0,225 0,220 0,200 0,190 0,100
No intervalo de 4 a 6 minutos a velocidade média da reação, em mol/L.min, é:
a) 0,010.
b) 0,255.
c) 0,005.
d) 0,100.
e) 0,200.
08) (UFRGS-RS) A isomerização de 1 mol de 1, 2 dicloro eteno foi realizada em um frasco fechado,
obtendo-se os seguintes valores de conversão em função do tempo:
tempo / min 0 10 20 30
Quantidade de matéria de A 1,00 0,90 0,81 0,73
Nos primeiros 10 minutos de reação a velocidade de isomerização em mol/min é:
a) 8,00 x 10– 3
.
b) 1,00 x 10
– 3
.
c) 9,00 x 10
– 2
.
d) 1,00 x 10– 2
.
e) 1,25 x 103
.
09) A decomposição da água oxigenada em determinadas condições experimentais produz 3,2 g de
oxigênio por minuto. A velocidade de decomposição do peróxido em mol/min é:
Dado: O = 16 u.
a) 0,05.
b) 0,10.
c) 0,20.
d) 1,70.
e) 3,40.
2](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-2-320.jpg)

![16) O Harber é um importante processo industrial para produzir amônia, conforme a reação:
N2 (g) + 3 H2 (g) 2 NH3 (g)
Colocados, num reator, nitrogênio e hidrogênio, obtiveram-se os seguintes dados em minutos e
mols/litro.
tempo ( min ) [N2] [H2] [H2]
0 0,50 1,50 -----
10 0,45 1,35 0,10
Calculando-se a velocidade média em função de NH3, N2, H2 e velocidade média da reação, obtêm-se,
respectivamente:
a) 0,01; – 0,005; – 0,015 e 0,005.
b) 0,01; 0,135; 0,045 e 0,005.
c) 0,01; – 0,130; – 0,045 e 0,005.
d) 0,01; 0,005; 0,015 e 0,005.
e) 0,10; 1,350; 0,450 e 0,005.
17) (Covest-2002) Óxidos de nitrogênio, NOx, são substâncias de interesse ambiental, pois são
responsáveis pela destruição de ozônio na atmosfera, e, portanto, suas reações são amplamente
estudadas. Num dado experimento, em um recipiente fechado, a concentração de NO2 em função do
tempo apresentou o seguinte comportamento:
0
concentração
tempo
O papel do NO2 neste sistema reacional é:
a) reagente.
b) intermediário.
c) produto.
d) catalisador.
e) inerte
18) (UnB-DF-Modificado) considere os estudos cinéticos de uma reação química e julgue os itens abaixo.
1) Toda reação é produzida por colisões, mas nem toda colisão gera uma reação.
2) Uma colisão altamente energética pode produzir uma reação.
3) Toda colisão com orientação adequada produz uma reação.
4) A velocidade média de uma reação pode ser determinada pela expressão:
v =
quantidade dos produtos
quantidade dos reagentes
Assinalando V para verdadeiro e F para falso e, lendo de cima para baixo, teremos:
a) V, V, F, F.
b) V, V, V, F.
c) F, V, F, F.
d) V, F, V, F.
e) V, V, V, V.
4](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-4-320.jpg)
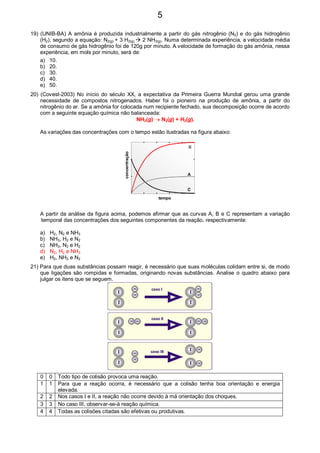




![39) Em qual das condições seguintes a velocidade da reação Zn(s) + 2 H+
(aq) Zn2+
(aq) + H2(g) é maior?
[H+
(aq)] Zn(s)
a) 1.0 pó
b) 1,0 lâmina
c) 1,0 raspas
d) 2,0 pó
e) 2,0 raspas
40) (PUC-RS) responder à questão com base no esquema a seguir, que representa situações em
comprimidos antiácidos efervescentes de mesma constituição reagem em presença de água.
20°C 20°C 20°C80°C 10°C
Pelo exame do esquema, pode-se afirmar que as reações que ocorrem em menor tempo do que a do
frasco I, são as dos frascos:
a) II e III.
b) II e IV.
c) II e V.
d) III e IV.
e) III e V.
41) Quais dos itens seguintes, associados, aumentam a velocidade da reação entre o ferro metálico e o
ácido clorídrico?
I. Ferro em lâminas.
II. Ferro finamente dividido.
III. Ácido clorídrico 6 mols/L.
IV. Ácido clorídrico 1 mol/L.
a) III e IV.
b) I e III.
c) II e III.
d) I e II.
e) II e IV.
42) O metal ferro reage com uma solução aquosa de HCl, originando gás hidrogênio e cloreto de ferro II.
Assinale a alternativa que indica a reação mais rápida entre o ferro e uma solução aquosa de HCl
1,0mol/L.
a) um prego de ferro, a 25°C.
b) um prego de ferro, a 40°C.
c) ferro em pó, a 40°C.
d) ferro em pó, a 25°C.
e) essa reação não depende da superfície de contato ou da temperatura.
43) (MACKENZIE-SP) É correta afirmar que as velocidades das reações dos compostos gasosos nos
sistemas contido em I e II abaixo, sob a ação de êmbolos, são, respectivamente:
A A’ B C
a) A > A’ e B > C.
b) A > A’ e C > B.
c) A’ = A e C > B.
d) A’ > A e C > B.
e) A’ > A e B = C.
10](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-10-320.jpg)



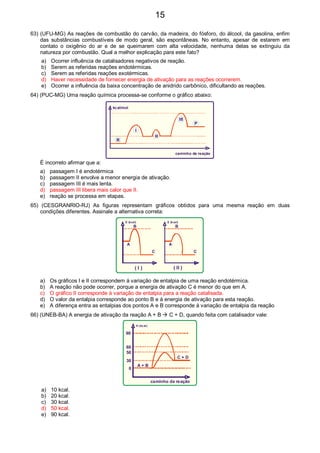
![67) (Covest-2006) José havia descoberto que, ao penetrar na corrente sangüínea e atingir o cérebro, o
ânion Pp−
é capaz de se associar a dois tipos de neurotransmissores, recA e recB, originando a
seguinte seqüência de reações elementares:
a) Pp−
+ recA recA−
+ Pp rápida
b) recA−
+ recB recA-recB−
lenta
c) recA-recB−
+ Pp recA + recB-Pp−
rápida
O recA−
causa contrações involuntárias, isto é, um tique nervoso que faz que a pessoa fique piscando
de forma insistente e involuntária o olho direito. O produto recB-Pp é que causa, efetivamente, a
sudorese e a tremedeira que Milton estava apresentando.
Considere as seguintes afirmações.
0 0 A reação global para o processo é: Pp
−
+ recB recB-Pp
−
.
1 1 Todas as etapas são bimoleculares e, portanto, reações com cinética de primeira
ordem.
2 2 A velocidade da reação global é determinada pela terceira etapa.
3 3 recA
−
e recA-recB
−
são intermediários de reação.
4 4 A lei de velocidade para reação global será: v=k[recA
−
]
m
[recB]
n
.
0-0) Verdadeiro. A reação global é a soma das três etapas.
1-1) Falso. Se as reações são bimoleculares, a cinética é de segunda ordem.
2-2) Falso. A velocidade da reação é determinada pela velocidade da etapa lenta (2ª etapa).
3-3) Verdadeiro. Intermediários de reação são formados em uma etapa e consumidos em etapas subseqüentes.
4-4) Falso. Intermediários de reação não podem aparecer na lei de velocidade global.
68) (Covest-2007) A queima de combustíveis nos automóveis, geralmente, não é completa, e um dos
produtos presentes nos gases de combustão é o monóxido de carbono, um gás extremamente tóxico.
Para minimizar a emissão desses gases para a atmosfera, os automóveis possuem um conversor
catalítico que acelera a reação:
CO(g) + ½O2(g) CO2(g)
No entanto, a reação ocorre em várias etapas, algumas das quais se encontram a seguir:
CO(g) + O2(g) CO2(g) + O(g) (I)
CO(g) + O(g) + M(s) CO2(g) + M(s) (II)
Ambas as etapas possuem energia de ativação positiva, porém a energia de ativação da etapa I é
muito maior que a da etapa II.
Considere o processo descrito e assinale a alternativa correta.
a) Um aumento de temperatura diminui a velocidade da etapa I e aumenta a velocidade da etapa II.
b) Para concentrações iguais dos reagentes, a qualquer temperatura, a etapa II é mais rápida que a
etapa I.
c) Com base na reação global, podemos dizer que a mesma é de segunda ordem, já que somente
dois reagentes são envolvidos na reação.
d) M não pode ser considerado um catalisador, uma vez que ele participa na etapa II.
e) Se dobrarmos a pressão parcial de monóxido de carbono, a velocidade da etapa II deverá dobrar;
porém, a velocidade da etapa I deverá diminuir, já que sua energia de ativação é maior.
69) A equação X + 2 Y XY2 representa uma reação, cuja equação da velocidade é:
v = k . [X] . [Y]
Indique o valor da constante de velocidade, para a reação dada, sabendo que, quando a concentração
de X é 1 mol/L e a de Y é 2 mol/L, a velocidade da reação é de 3 mol/L.min.:
a) 3,0.
b) 1,5.
c) 1,0.
d) 0,75.
e) 0,5.
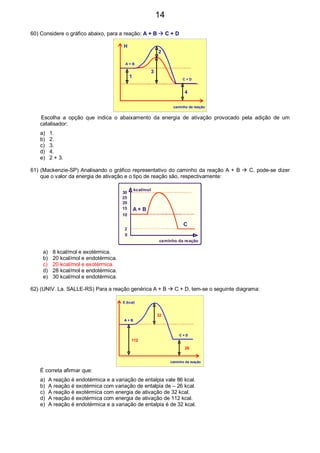
70) (Covest-2000) A lei de velocidade para a reação 2 NO(g ) + O2 (g ) 2 NO2 (g ) é:
v = k [NO]
2
[O2]
Se triplicarmos as concentrações de NO e O2 ao mesmo tempo, quantas vezes mais rápida será a
reação?
16](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-16-320.jpg)
![71) Numa reação temos x mol/L de H2 e y mol/L de O2. A velocidade da reação é V1. Se dobrarmos a
concentração de hidrogênio e triplicarmos a de oxigênio, a velocidade passa a V2. Qual relação entre V1
e V2?
a) V2 = 2 V1.
b) V2 = 4 V1.
c) V2 = 12 V1.
d) V2 = 24 V1.
e) V2 = 6 V1.
72) Na reação de dissociação térmica do HI(g), a velocidade de reação é proporcional ao quadrado da
concentração molar do HI. Se triplicarmos a concentração molar do HI, a velocidade da reação:
a) aumentará 6 vezes.
b) aumentará 9 vezes.
c) diminuirá 6 vezes.
d) diminuirá 9 vezes.
e) diminuirá 3 vezes.
73) A reação 2 A + B P, apresenta uma lei de velocidade expressa por v = k [A]
2
. Se a concentração de
reagente A for mantida constante e a de B for duplicada, a velocidade da reação fica multiplicada por
um fator igual a:
a) 0.
b) 1.
c) 2.
d) 3.
e) 4.
74) A reação NO2(g) + CO(g) CO2(g) + NO(g) é de segunda ordem em relação ao NO2(g) e de ordem zero em
relação ao CO(g). Em determinadas condições de temperatura e pressão, essa reação ocorre com
velocidade v. Se triplicarmos a concentração de NO2(g) e duplicarmos a concentração de CO(g), a nova
velocidade de reação v’ será igual a:
a) 3v.
b) 6v.
c) 9v.
d) 12v.
e) 18v.
75) Dada a equação da reação elementar H2 + Cl2 2 HCl, se reduzirmos simultaneamente a
concentração de H2 e Cl2 à metade, mantendo-se constantes todos os outros fatores, a velocidade da
reação:
a) quadruplica.
b) reduz-se a um quarto da inicial.
c) dobra.
d) reduz-se à metade.
e) permanece igual à inicial.
76) (UNAERP-SP) Se tivermos em um recipiente, à temperatura ambiente, dois gases prontos para reagir,
segundo a reação elementar abaixo, o que acontecerá com a velocidade de reação dos gases se, em
um dado momento, apenas dobrarmos as concentrações molares dos gases:
A(g) + 3 B(g) 2 C(g)
a) A velocidade da reação aumentará 16 vezes.
b) A velocidade da reação duplicará.
c) A velocidade da reação permanecerá a mesma.
d) A velocidade da reação será reduzida à metade.
e) A velocidade da reação aumentará 4 vezes.
77) (FUVEST-SP) O estudo cinético, em fase gasosa, da reação representada por NO2 + CO CO2 + NO
mostrou que a velocidade da reação não dependa da concentração de CO, mas depende da
concentração de NO2 elevada ao quadrado. Esse resultado permite afirmar que:
a) o CO atua como catalisador.
b) o CO é desnecessário para a conversão do NO2 em NO.
c) o NO2 atua como catalisador.
d) a reação deve ocorrer em mais de uma etapa.
e) a velocidade da reação dobra se a concentração inicial do NO2 for duplicada.
17](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-17-320.jpg)
![78) (FEPAR-PR) Analise a reação elementar 2 A + B C e o seu diagrama de energia na ausência e
presença de catalisador, representado a seguir:
H (kcal)
C
caminho da reação
2 A + B
25
50
15
Sobre eles (reação e diagrama), são feitas as seguintes afirmações:
I. O catalisador aumenta a velocidade da reação, provocando a diminuição da sua energia de
ativação.
II. Ao se dobrar, simultaneamente, as concentrações, mol/L, de A e B, a velocidade da reação irá
quadruplicar.
III. O valor da energia de ativação da reação inversa sem catalisador é 75 kcal.
IV. A adição do catalisador altera a variação de entalpia da reação.
Estão corretas somente:
a) II e IV.
b) I e III.
c) II e III.
d) I e IV.
e) II, III e IV.
79) O óxido nítrico reage com hidrogênio, produzindo nitrogênio e vapor de água de acordo com a reação:
2 NO (g) + 2 H2 (g) N2 (g) + 2 H2O (g)
Acredita-se que essa reação ocorra em duas etapas:
2 NO + H2 N2O + H2O (lenta)
N2O + H2 N2 + H2O (rápida)
De acordo com esse mecanismo, a expressão da velocidade da reação é:
a) v = k [NO]
2
[H2}.
b) v = k [NO2][H2O].
c) v = k [NO][H2].
d) v = k [N2][H2O].
e) v = k [N2][H2O]2
.
80) (Covest-2007) Sobre os parâmetros e variáveis que governam a velocidade de reações químicas,
podemos afirmar que:
0 0 em geral, as reações aumentam de velocidade com o aumento da temperatura.
1 1 em geral, as reações diminuem de velocidade com o aumento da concentração dos
reagentes em solução.
2 2 a uma dada temperatura, a velocidade de uma reação será maior quanto menor for sua
energia de ativação.
3 3 o aumento da pressão parcial dos reagentes, provoca um aumento na velocidade de uma
reação entre substâncias no estado gasoso.
4 4 um catalisador atua aumentando a energia de ativação para uma determinada etapa de
uma reação química.
Resposta: VFVVF
Justificativa:
0-0) Verdadeiro: Com o aumento da temperatura, um maior número de espécies reativas tem energia maior que a energia de
ativação da reação (segundo a teoria das colisões) e com isto a reação aumenta de velocidade.
1-1) Falso: Com o aumento de concentração, aumenta a freqüência de colisão entre as espécies reativas e com isso aumenta a
velocidade.
2-2) Verdadeiro: A energia de ativação corresponde a uma barreira energética que as espécies reativas devem suplantar para que
a reação ocorra. Quanto menor esta barreira, maior a velocidade da reação.
3-3) Verdadeiro: O aumento de pressão, para gases, corresponde em um aumento de concentração, e isto causa um aumento na
velocidade das reações.
4-4) Falso: O catalisador atua alterando o caminho de reação, por um caminho de menor energia de ativação.
18](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-18-320.jpg)
![81)(Covest-2003)A reação do óxido de nitrogênio com cloro, descoberta em 1914, foi a primeira reação
gasosa elementar trimolecular: 2NO(g) + Cl2(g) → 2NOCl(g). Sobre a cinética desta reação, podemos
afirmar que:
0 0 A variação da concentração de NO com relação ao tempo pode ser representada pelo
gráfico:
concentraçãoNO
tempo
1 1 A variação da concentração de Cl2 com relação ao tempo pode ser representada pelo
gráfico:
concentraçãoCl2
tempo
2 2 A variação da concentração de NOCl com relação ao tempo pode ser representada pelo
gráfico:
concentraçãoNOCl
tempo
3 3 Se duplicarmos a concentração de NO a velocidade da reação aumenta quatro vezes.
4 4 Se duplicarmos a concentração de Cl2 a velocidade da reação aumenta quatro vezes.
0-0) Sendo NO um reagente, sua concentração diminui com o passar do tempo como ilustrado no gráfico.
1-1) Sendo Cl2 um reagente, sua concentração diminui com o passar do tempo e o gráfico mostra sua concentração
aumentando à medida que o tempo passa.
2-2) Sendo NOCl um produto, sua concentração aumenta com o passar do tempo como mostrado no gráfico.
3-3) Desde que a reação é elementar sua lei de velocidade será: v = k [NO]2
[Cl2], onde k é a constante de
velocidade e os colchetes representam concentrações em mol por litro. Portanto, se duplicarmos a
concentração de NO a velocidade da reação aumenta quatro vezes.
4-4) De acordo com o item 3-3), se duplicarmos a concentração de Cl2 a velocidade da reação duplica.
82) (UNICAP-2007/Q2)
0 0 O aumento da temperatura provoca um aumento da rapidez das transformações
químicas.
1 1 Para promover uma melhor condição de ocorrência de uma reação química, é primordial
que as moléculas dos reagentes sejam postas em contato do modo mais eficaz possível.
2 2 Pode-se afirmar que quanto menor for a energia de ativação, maior será a velocidade de
uma reação química.
3 3 As reações nas quais os catalisadores atuam ocorreriam mesmo nas ausências dessas
substâncias.
4 4 A explicação da utilização de ouro no recobrimento dos contatos eletrônicos das placas
dos computadores está relacionado com o potencial eletroquímico dos metais.
19](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-19-320.jpg)
![83) (Covest-2008) O íon hipoclorito é o principal ingrediente da água sanitária, que é amplamente
empregada como alvejante. A reação de hipoclorito com corantes produz substâncias incolores. Analise
os resultados abaixo, obtidos para a reação de um corante com hipoclorito, e assinale a alternativa
correta.
experimento [ClO–
] (mol/L) [corante] (m ol/L) velocidade Inicial (mol/L)
1 1,7 x 10
–3
1,7 x 10
–2
1,7 x 10
4
2 3,4 x 10
–3
1,7 x 10
–2
3,4 x 10
4
3 1,7 x 10
–3
3,4 x 10
–2
3,4 x 10
4
a) A reação é de primeira ordem em relação ao hipoclorito e de segunda ordem em relação ao
corante.
b) A reação é de primeira ordem em relação a ambos os reagentes.
c) A reação é de segunda ordem em relação a ambos os reagentes
d) A constante de reação é 121 mol-1
L s-1
.
e) A constante de reação é 121 mol L-1
s-1
.
84) (Covest-2008) A reação de nitrogênio atmosférico com oxigênio produz óxido de nitrogênio:
N2(g) + O2(g) → 2NO(g)
Esta reação é muito lenta em temperatura ambiente, tornando-se importante somente a elevadas
temperaturas, como as presentes em motores de combustão interna. Este óxido participa em diversas
reações na atmosfera, levando à formação de vários poluentes, com forte impacto ambiental. Algumas
das etapas elementares propostas para esta reação encontram-se abaixo:
N2(g) + O(g) → NO(g) + N(g) (Etapa 1)
N(g) + O2(g) → NO(g) + O(g) (Etapa 2)
O(g) é intermediário presente na combustão em motores. A Etapa (1) é considerada determinante da
velocidade da reação, pois possui elevada energia de ativação (317 kJ·mol
–1
), muito maior do que na
Etapa (2). Sobre esse tema, avalie as seguintes afirmativas:
0 0 A Etapa (1) é mais afetada por um aumento de temperatura do que a Etapa (2).
1 1 A Etapa (2) é de segunda ordem.
2 2 Como a Etapa (1) é a determinante da velocidade da reação, espera-se que a reação
global seja de segunda ordem em relação ao nitrogênio.
3 3 Um aumento na temperatura reacional deve diminuir a velocidade da reação, uma vez
que a energia de ativação é muito elevada.
4 4 Um aumento na pressão parcial do oxigênio (O2) deve diminuir a velocidade da reação,
uma vez que ele não participa da Etapa (1).
0 – 0 Verdadeiro: A reação mais afetada pela temperatura é a de maior energia de ativação.
1 – 1 Verdadeiro: Primeira ordem em N e primeira ordem em O2.
2 – 2 Falso: A reação deve ser de primeira ordem em relação ao nitrogênio.
3 – 3 Falso: O aumento de temperatura aumenta a velocidade da reação.
4 – 4 Falso: O fato de não participar na etapa lenta, não implica diminuir a velocidade da reação.
85) A reação expressa pela equação 2 PQ + 2 R2 P2 + 2 R2Q, a 100°C apresenta o seguinte
mecanismo:
I. 2 PQ + R2 P2Q + R2Q (etapa lenta)
II. P2Q + R2 P2 + R2Q (etapa rápida)
Analise as afirmações:
0 0 Dobrando a concentração do PQ, a velocidade da reação será quadruplicada.
1 1 Dobrando a concentração do R2, a velocidade da reação também dobrará.
2 2 Triplicando a concentração do PQ e do R2 a velocidade da reação ficará nove vezes maior.
3 3 A equação da velocidade de reação é v = k [PQ]
2
[R2]
2
.
4 4 A reação é elementar.
20](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-20-320.jpg)
![86) (SANTA CASA) A reação hipotética 2 X + 2 Y P + Q poderá ocorrer segundo o seguinte mecanismo:
• X + Y Z + W ................................. V1
• X + Z P .........................................V2
• W + Y Q ........................................V3
• (soma): 2 X + 2 Y P + Q ...............V4
Onde V são as velocidades das reações expressas em mol/L.s. Admitindo que V1 = V3 > V2, a
velocidade global, V4, deverá ser mais próxima de:
a) V1 + V2.
b) V2.
c) V3.
d) V3 – V2.
e) 2 V1 + V2.
87) (Covest-2004)Um mecanismo proposto para a decomposição do gás N2O consiste nas seguintes etapas
elementares:
1ª etapa:
2ª etapa:
N N
N N
O
OO
O
2
2 2
2 2 2
k
k1
+
++
Sabendo-se que a lei da velocidade obtida experimentalmente é: v = k [N2O], pode-se afirmar que:
a) a 1ª etapa é a etapa determinante da velocidade de reação e, por isso, k2 >> k1.
b) a 1ª etapa é a etapa determinante da velocidade de reação e, por isso, k1 >> k2.
c) a 2ª etapa é a etapa determinante da velocidade de reação e, por isso, k2 >> k1.
d) a 2ª etapa é a etapa determinante da velocidade de reação e, por isso, k1 >> k2.
e) a reação global é representada pela equação química: 2 N2O + O 2 N2 + 3/2 O2.
88) (ESPCEX-SP) No processo industrial da produção de uma substância “F”, onde a energia total dos
produtos é menor do que a da matéria-prima “A”, são necessárias várias etapas, como descritas nas
equações abaixo:
I) A – B
II) B + C D + E (lenta)
III) E + A 2 F
Entre os gráficos, “energia x caminho da reação”, citados abaixo, o que melhor representa o processo
global da produção de “F” é:
E
E
E
E
E
C.R
C.R
C.R
C.R
C.R
I II III
IV V
a) I.
b) II.
c) III.
d) IV.
e) V.
89) (Fuvest-SP) O estudo de certa reação química é representada por 2 A (g) + 2 B (g) C (g) onde A,
B e C significam as espécies químicas que são colocadas para reagir. Verificou-se experimentalmente,
numa certa temperatura, que a velocidade dessa reação quadruplica com a duplicação da concentração
da espécie A, mas não depende das concentrações das espécies B e C. Assinale a opção que contém,
respectivamente, a expressão correta da velocidade e o valor da ordem da reação:
a) v = k [A]
2
{B]
2
e 4.
b) v = k [A]
2
[B]
2
e 3.
c) v = k [A]2
[B]2
e 2.
d) v = k [A]2
e 4.
e) v = k [A]2
e 2.
21](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-21-320.jpg)
![90) A cinética da reação hipotética: 2 A + 3 B D + 2 C foi estudada, obtendo-se a seguinte tabela:
Experiência [A] x 10
2
inicial [B] x 10
2
inicial V inicial de formação de D ( mol / min )
1 1,0 1,0 2,0
2 2,0 1,0 4,0
3 3,0 1,0 6,0
4 1,0 2,0 8,0
A lei da velocidade para a reação hipotética é fornecida pela equação:
a) v = k [A]2
[B]3
.
b) v = k [A]2
[B]2
.
c) v = k [A]2
[B] .
d) v = k [A] [B]2
.
e) v = k [A]
91) (Covest-2003) Em determinadas condições de temperatura e pressão, a decomposição térmica do éter
dimetílico (ou metoxietano ou oxibismetano), dada pela equação:
(CH3)2O(g) CH4(g) + H2(g) + CO(g)
Exibe a seguinte dependência da velocidade com a concentração:
Experimento Concentração inicial de
(CH3)2O em mol L
–1
Velocidade inicial em 10
9
mol L
–1
s
–1
1 0,20 1,60
2 0,40 6,40
3 0,60 14,4
Considerando que a concentração da espécie química X seja denominada como [X], a velocidade (v)
para essa reação será expressa como:
a) v = k [(CH3)2O]
b) v = k [CH4][H2][CO]
c) v = k
d) v = k [(CH3)2O]
2
e) v = k
]O)CH[(
]CO][H][CH[
23
24
92) (UFPB) A tabela abaixo indica valores das velocidades da reação e as correspondentes concentrações
em mol/L dos reagentes em idênticas condições, para o processo químico representado pela equação:
3 X + 2 Y Z + 5 W
v/mol.L
– 1
min
– 1
[X] [Y]
10 5 10
40 10 10
40 10 20
A equação de velocidade desse processo é:
a) v = k.[X]3
.[Y]2
.
b) v = k.[X]
2
.[Y]
2
.
c) v = k.[X]
0
.[Y]
2
.
d) v = k.[X]2
.[Y]0
.
e) v = k.[X]2
.[Y]3
.
93) (Uespi) A reação que ocorre utilizando os reagentes A e B é de terceira ordem. Para essa reação não é
possível aplicar a expressão da lei de velocidade:
a) v = k [A] [B]
2
.
b) v = k [A]
3
.
c) v = k [B]
3
.
d) v = k [A]2
[B].
e) v = k [A]3
[B]3
.
22](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-22-320.jpg)
![A tabela abaixo mostra a reação entre a concentração molar de um reagente X e a velocidade inicial da
reação.
[X] (mol/L) v (mol/L.min)
1ª experiência 0,03 0,6
2º experiência 0,06 1,2
3ª experiência 0,09 1,8
As questões 94 e 95 devem ser respondidas com base nestas informações:
94) A lei da velocidade da reação, em função da concentração molar de X é dada por:
a) v = k [X].
b) v = k [X]2
.
c) v = k [X]3
.
d) v = k [X] – 2
.
e) v = k [X]1/2
.
95) O valor da constante de velocidade, k, é igual a:
a) 0,02 h –1
.
b) 0,05 h –1
.
c) 20 h –1
.
d) 2 h –1
.
e) 0,5 h –1
.
96) (Covest-2006) José havia descoberto que, ao penetrar na corrente sangüínea e atingir o cérebro, o
ânion Pp
−
é capaz de se associar a dois tipos de neurotransmissores, recA e recB, originando a
seguinte seqüência de reações elementares:
d) Pp
−
+ recA recA
−
+ Pp rápida
e) recA−
+ recB recA-recB−
lenta
f) recA-recB−
+ Pp recA + recB-Pp−
rápida
O recA
−
causa contrações involuntárias, isto é, um tique nervoso que faz que a pessoa fique piscando
de forma insistente e involuntária o olho direito. O produto recB-Pp é que causa, efetivamente, a
sudorese e a tremedeira que Milton estava apresentando.
Considere as seguintes afirmações.
0 0 A reação global para o processo é: Pp
−
+ recB recB-Pp
−
.
1 1 Todas as etapas são bimoleculares e, portanto, reações com cinética de primeira
ordem.
2 2 A velocidade da reação global é determinada pela terceira etapa.
3 3 recA
−
e recA-recB
−
são intermediários de reação.
4 4 A lei de velocidade para reação global será: v=k[recA
−
]
m
[recB]
n
.
97) (PUC-MG) No estudo da cinética da reação 2 NO + 2 H2 N2 + 2 H2O, à temperatura de 700°C, foram
obtidos os seguintes dados, de acordo com a tabela abaixo:
[H2] [NO] Velocidade inicial
1 x 10
– 3
1 x 10
– 3
3 x 10
– 5
2 x 10
– 3
1 x 10
– 3
6 x 10
– 5
2 x 10
– 3
2 x 10
– 3
24 x 10
– 5
Analisando os resultados, é correto afirmar que a lei da velocidade para essa reação é:
a) v = k[H2][NO]
2
.
b) v = k[H2][NO].
c) v = k[H2]2
.
d) v = k[H2]
2
[NO]
2
.
e) v = k[NO]2
.
23](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-23-320.jpg)
![98) (Rumo-2004) Uma reação que pode ocorrer no ar poluído é:
NO2(g) + O3(g) NO3(g) + O2(g),
Três experimentos foram realizados a 25°C, p ara estudar a cinética dessa reação:
Experimento [NO2]INICIAL [O3] INICIAL velocidade inicial (mol/L.s)
1 5,0 x 10
– 5
1,0 x 10
– 5
2,2 x 10
– 2
2 5,0 x 10
– 5
2,0 x 10
– 5
4,4 x 10
– 2
3 2,5 x 10
– 5
2,0 x 10
– 5
2,2 x 10
– 2
Utilizando os dados experimentais da tabela acima, determine a expressão da lei da velocidade, a
ordem da reação e o valor da constante de velocidade, respectivamente.
a) v = k [O3]; ordem = 1 e k = 2,2 x 10 7
s – 1
.
b) v = k [NO2]; ordem = 1 e k = 4,4 x 10 7
s – 1
.
c) v = k [NO2]; ordem = 2 e k = 2,2 x 10 7
s – 1
.
d) v = k [NO2] [O3]; ordem = 2 e k = 4,4 x 10 7
s – 1
.
e) v = k [NO2] + [O3]; ordem = 2 e k = 4,4 x 10 7
s – 1
.
99) (Covest-2004) A figura abaixo mostra como a concentração de um reagente “A” varia com o tempo em
duas reações que apresentam cinética de primeira ordem. K1 e K2 são as constantes de velocidade.
K
K
1
2
A[ ]
tempo (s)
concentraçãomolardereagente[A]
0
0 0 A lei de velocidade das reações em estudo é dada por v = K.[A].
1 1 A unidade da constante de velocidade é dada por mol/L.s.
2 2 Pelo gráfico dado, K1 < K2. e, portanto, a reação 1 é mais rápida que a reação 2.
3 3 O tempo de meia-vida da reação 2 é menor que o da reação 1.
4 4 Se a concentração de “A” duplicar, a velocidade da reação quadruplicará.
0 – 0 Sim, a reação é de primeira ordem.
1 – 1 Falso, pois a unidade da constante de velocidade de uma reação de primeira ordem é 1/s.
2 – 2 Sim, pois no mesmo tempo maior variação [A] em 2 do que em 1, isto implica que K2 > K1.
3 – 3 Falso, pois a constante e a meia-vida são inversamente proporcionais, então se K2 > k1 teremos v1 > v2.
4 – 4 Falso, pois se a concentração de “A” duplicar a velocidade da reação duplicará.
100)(FUVEST-SP) Em solução aquosa ocorre a transformação:
H2O2 + I
–
+ 2 H
+
2 H2O + I2
(reagentes) (produtos)
Em quatro experimentos, mediu-se o tempo decorrido para a formação de mesma concentração de I2,
tendo-se na mistura de reação as seguintes concentrações iniciais de reagentes:
2 2
H HO I +-
I
II
III
IV 0,25
0,25
0,25
0,25
0,25
0,25
0,25
0,25
0,25
0,17
0,17
0,17
56
56
87
85
concentração inicial
em mol/L
tempoexperi-
mento
Esses dados indicam que a velocidade da reação considerada depende apenas da concentração de:
a) H2O2 e I
–
.
b) H2O2 e H+
.
c) H2O2.
d) H+
.
e) I –
.
24](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-24-320.jpg)
![101)(Fuvest-SP) nas condições ambientes, foram realizados três experimentos, com aparelhagem idêntica,
nos quais se juntou Na2CO3 sólido, contido em uma bexiga murcha, a uma solução aquosa de HCl
contida em um erlenmeyer. As quantidades adicionadas foram:
Solução de H Cl
Experimento
Massa de
Na C O3 g( )
Volume
( mL )
Concentração
( mol/L)
E
E
E 1
2
3
2
1,06
1,06
1,06
100
100
100
0,30
0,40
0,50
HCl
Na C O32
Ao final dos experimentos, comparando-se os volumes das bexigas, observa-se que:
Dado: Na2CO3 = 106 g/mol.
a) A bexiga de E1 é a mais cheia.
b) A bexiga E2 é a mais cheia.
c) A bexiga E3 é a mais cheia.
d) A bexiga E1 é a menos cheia.
e) As três bexigas estão igualmente cheias.
102)(Covest-2005) Quando a concentração de 2-bromo-2-metilpropano, C4H9Br dobra, a velocidade da
reação abaixo aumenta por um fator de 2. se as concentrações de C4H9Br e OH –
são dobradas, o
aumento é o mesmo: um fator de 2. Com relação a esses dados, analise as afirmativas a seguir.
4 4C CH H9 9( ) ( )( )( )+ +OH OHBr Braq aqaqaq
-
1) A lei da velocidade da reação pode ser escrita como: v = k [C4H9Br] [OH −
] e, portanto, a
reação é de segunda ordem.
2) A lei da velocidade da reação pode ser escrita como: v = k [C4H9Br] e, portanto, a reação é de
primeira ordem.
3) A lei da velocidade da reação pode ser escrita como: v = k [C4H9Br] e, portanto, a reação é
primeira ordem, com relação ao C4H9Br, e de ordem zero, com relação ao OH –
.
4) Se a concentração de íons OH1 – 1
triplicar, a velocidade da reação não se altera.
5) A meia-vida, t1/2, independe da concentração inicial dos reagentes.
Estão corretas:
a) 1, 2, 4 e 5 apenas.
b) 1, 3, 4 e 5 apenas.
c) 2, 3, 4 e 5 apenas.
d) 1 e 5 apenas.
e) 1, 2, 3, 4 e 5.
103)(UFSCar-SP) A decomposição do pentóxido de dinitrogênio é representada pela equação:
2 N2O5(g) 4 NO2(g) + O2(g)
Foram realizados três experimentos, apresentados na tabela:
experimento [N2O4] velocidade
I x 4z
II x/2 2z
III x/4 Z
A expressão da velocidade da reação é:
a) v = k[N2O4]0
b) v = k[N2O4]1/4
c) v = k[N2O4]1/2
d) v = k[N2O4]1
e) v = k[N2O4]2
25](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-25-320.jpg)
![104)(Urca-CE) Dada a seguinte reação genérica “2 A + B C” e o quadro cinético abaixo:
Experiência [A] mol/L [B] mol/L Velocidade (mol/L.s)
I 0,42 0,21 0,20
II 0,42 0,63 1,80
III 0,84 0,21 0,40
É correto afirmar:
a) é uma reação elementar.
b) a ordem global da reação é 2.
c) a lei de velocidade é v = k[A]2
[B].
d) a constante de velocidade é igual a 1.
e) a lei de velocidade é v = k[A][B]2
.
26](https://image.slidesharecdn.com/cineticaquimica-150610222305-lva1-app6892/85/Cineticaquimica-26-320.jpg)