Incorporar apresentação
Baixado 111 vezes


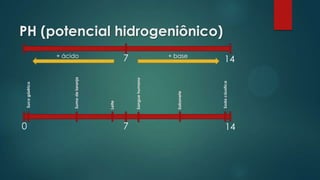





O documento descreve as características de ácidos e bases, incluindo seu sabor, pH e indicadores. Ele lista alguns ácidos e bases importantes e explica que a reação de neutralização entre um ácido e uma base produz um sal e água.






