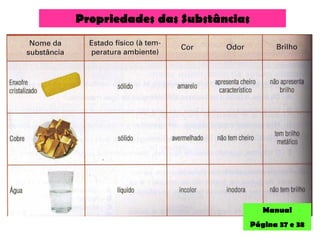
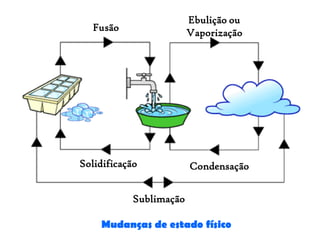
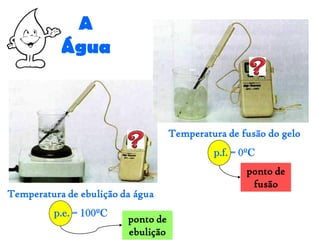
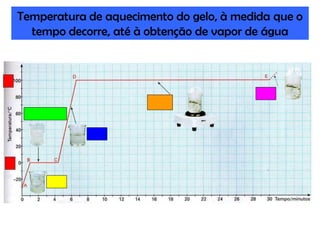
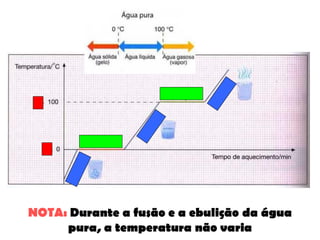
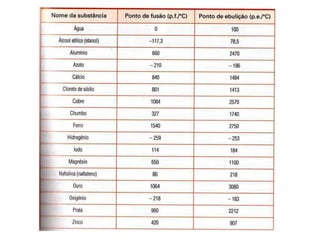
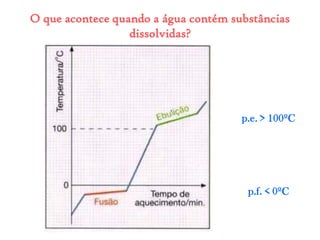
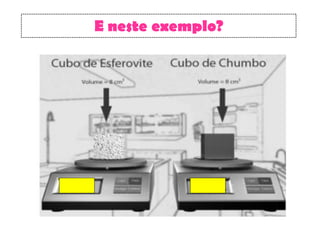
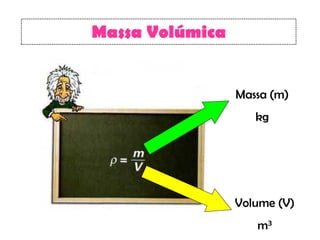
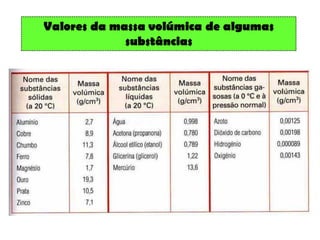
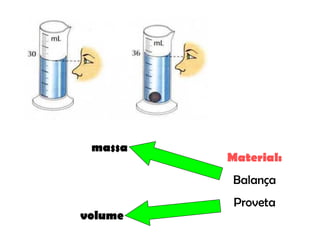
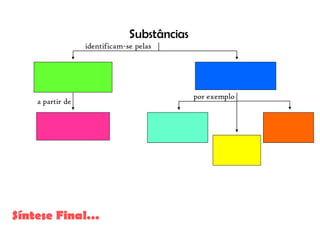
O documento discute as propriedades químicas e físicas das substâncias. Explica que as propriedades químicas identificam uma substância através de ensaios químicos, enquanto as propriedades físicas incluem ponto de fusão, ponto de ebulição e massa volúmica. Também descreve as mudanças de estado físico como fusão, vaporização e outros processos.