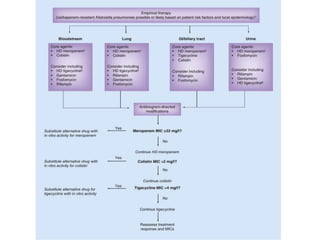
1) O documento discute a resistência bacteriana aos carbapenêmicos, especialmente as carbapenemases, e as abordagens para o tratamento de infecções causadas por bactérias produtoras dessas enzimas.
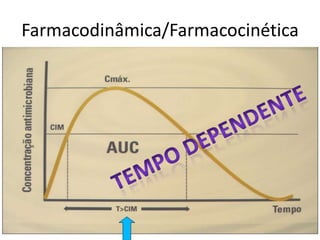
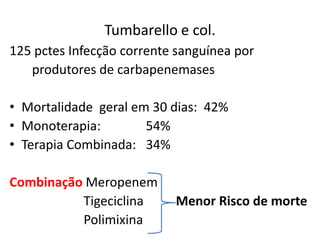
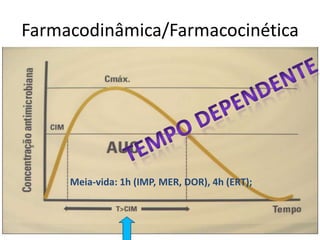
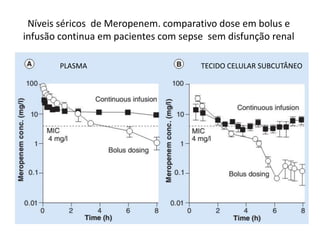
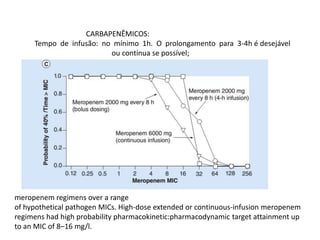
2) É enfatizada a importância da terapia combinada contendo altas doses de carbapenêmicos ou polimixina para o tratamento destas infecções.
3) As medidas de controle de infecção também são cruciais para conter a disseminação destes microrganismos resistentes.