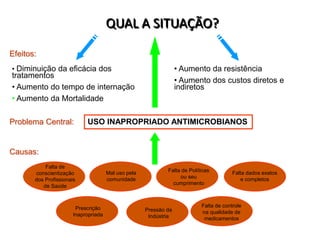
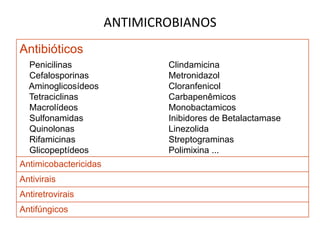
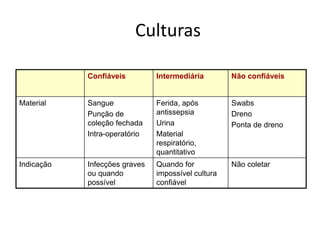
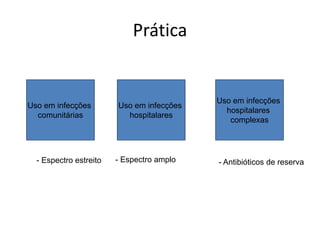
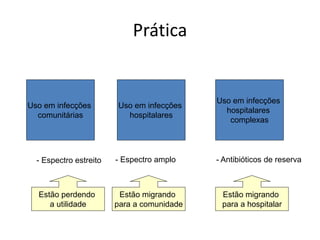
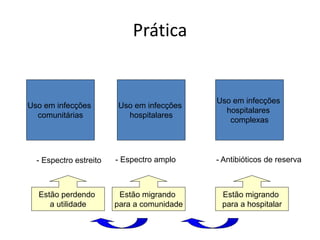
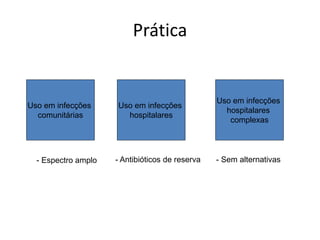
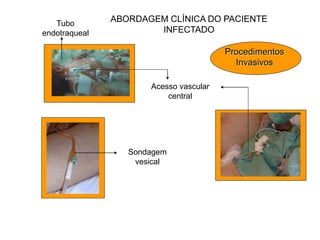
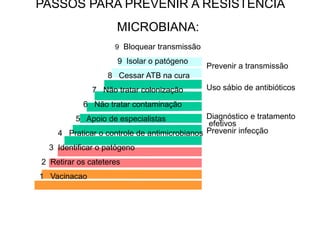
O documento discute o uso inapropriado de antimicrobianos e suas consequências, como aumento da resistência e da mortalidade. Ele apresenta as principais causas do uso inapropriado, como falta de conscientização, pressão da indústria farmacêutica e prescrição inadequada. Também fornece recomendações para instituir políticas de uso racional desses medicamentos, como otimizar a escolha e duração do tratamento.