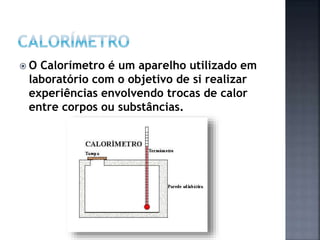
O documento discute conceitos-chave de calor e energia térmica. Explica que o calor específico indica a quantidade de calor necessária para elevar a temperatura de 1 grau de uma substância e fornece exemplos. Também define capacidade térmica como a razão entre a quantidade de calor trocado e a variação de temperatura resultante. Por fim, discute o uso do calorímetro em experimentos de troca de calor e as equações que regem essas trocas.