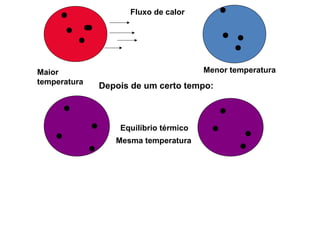
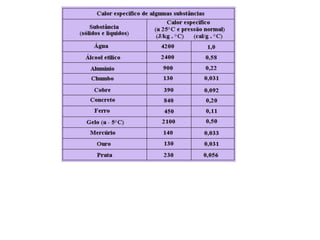
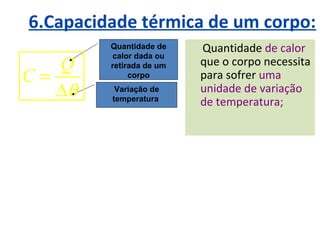
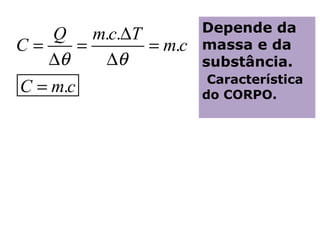
Calorimetria estuda a transferência de energia térmica entre sistemas. Quando um corpo está a uma temperatura maior que outro, o calor flui do mais quente para o mais frio até que alcancem a mesma temperatura. A quantidade de calor transferida depende da massa dos corpos e de sua capacidade térmica, definida como a quantidade de calor necessária para alterar sua temperatura em 1°C.