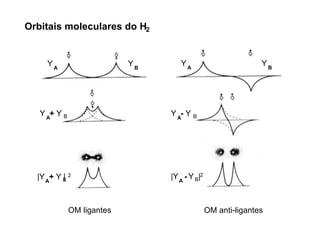
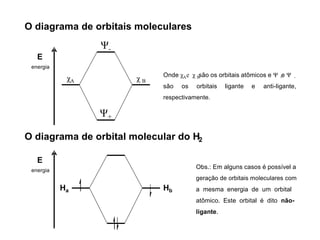
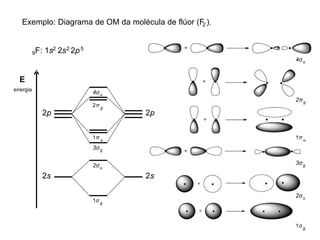
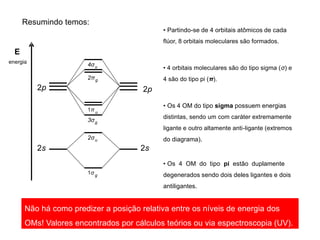
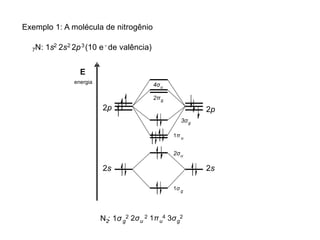
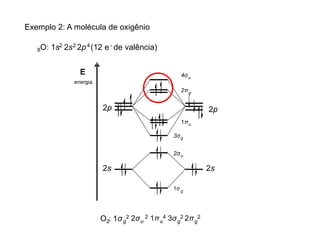
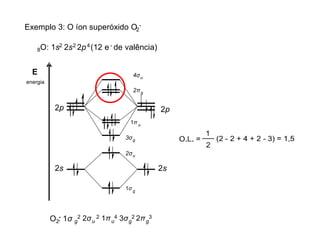
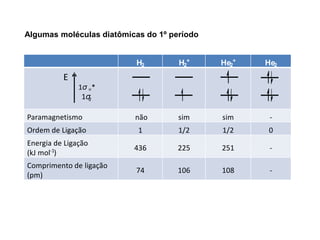
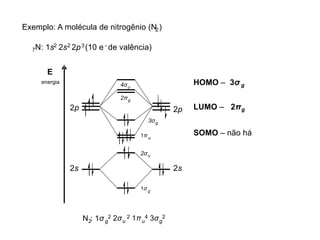
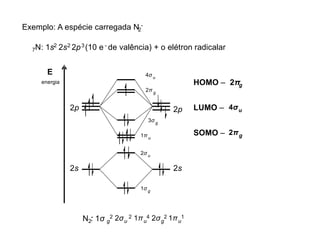
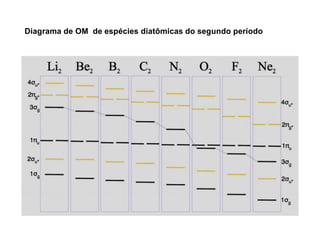
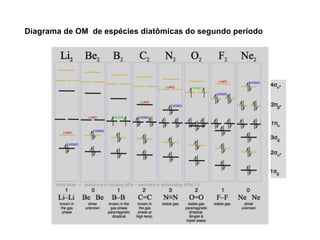
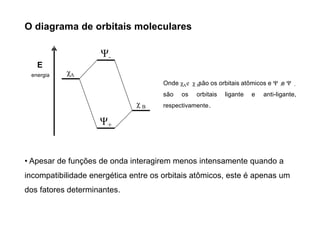
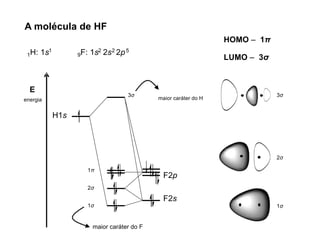
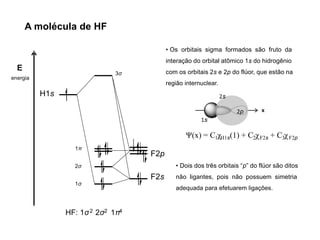
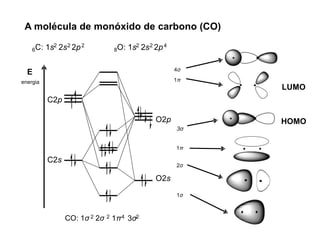
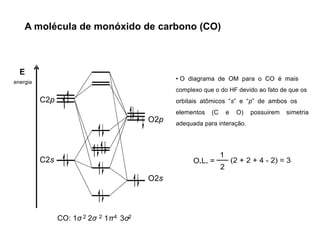
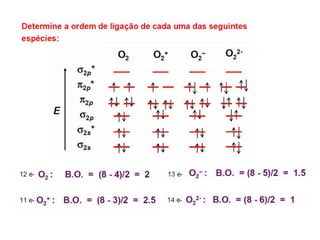
A teoria dos orbitais moleculares (COM) é uma abordagem que explica a formação de moléculas poliatômicas através da combinação de orbitais atômicos, levando em conta a distribuição eletrônica e a ordem de ligação. O documento também discute a formação de orbitais moleculares ligantes e anti-ligantes, a importância dos orbitais de fronteira nas reações químicas e a aplicação de diagramas de orbitais moleculares em diferentes moléculas diatômicas. Exemplos incluem a análise dos diagramas de H2, N2, O2 e CO, que ilustram como a energia e a simetria influenciam as propriedades químicas e físicas das moléculas.