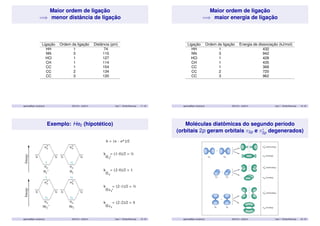
O documento discute a teoria do orbital molecular, explicando como orbitais atômicos se combinam para formar orbitais moleculares. Aborda conceitos como orbitais ligantes e antiligantes, ordem de ligação, diagramas de níveis de energia para várias moléculas diatômicas e poliatômicas, e como a teoria se estende para sólidos através da teoria de bandas.