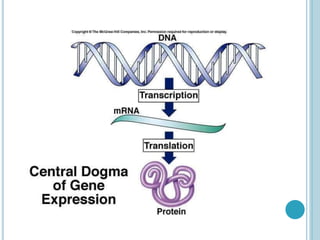
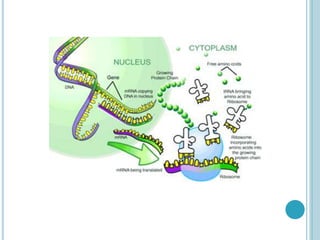
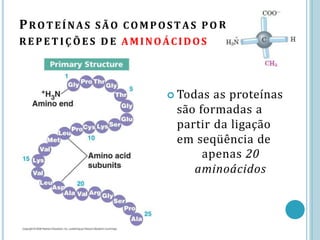
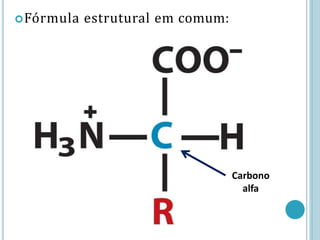
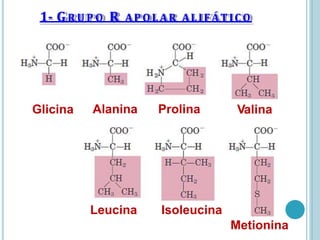
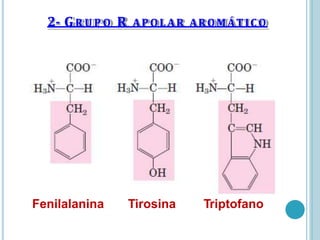
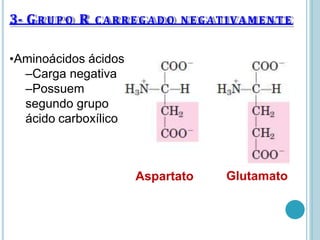
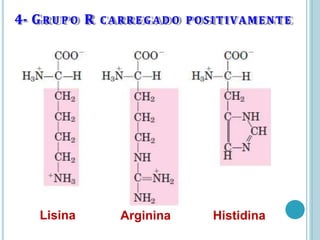
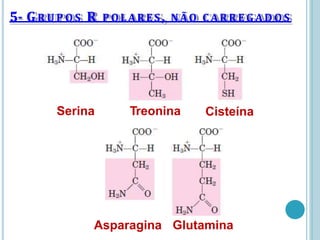
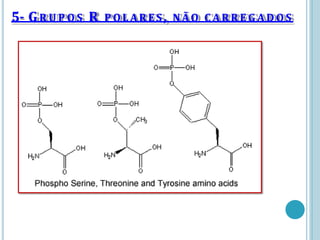
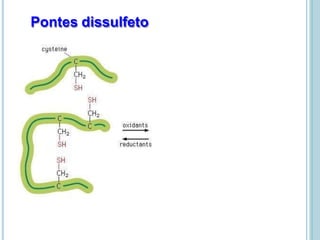
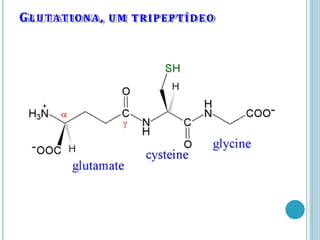
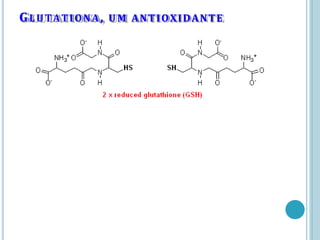
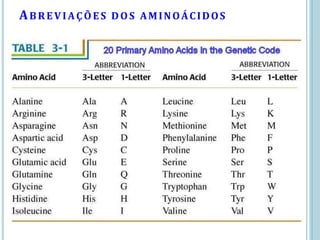
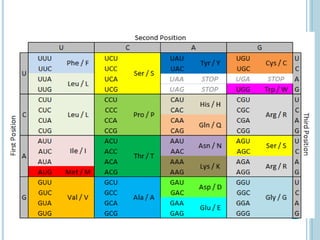
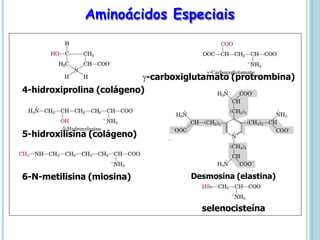
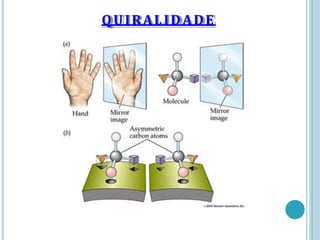
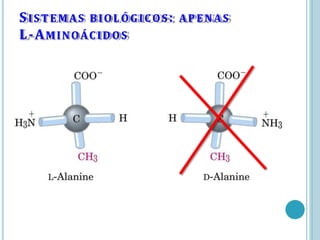
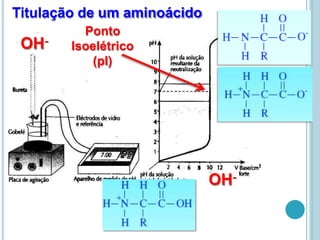
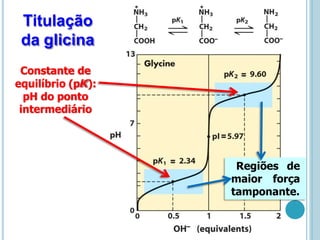
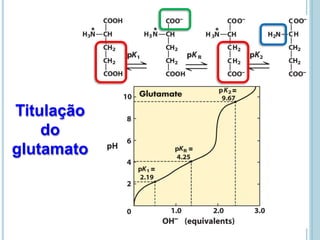
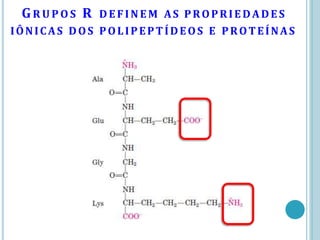
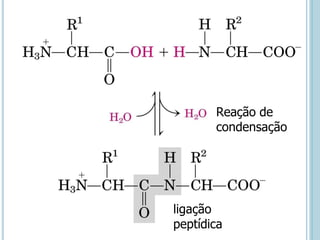
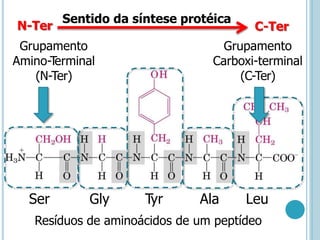
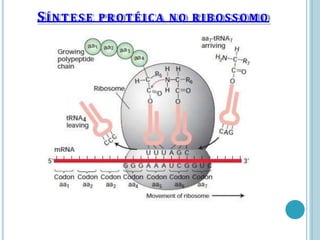
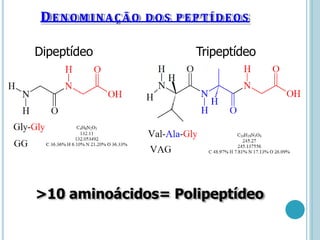
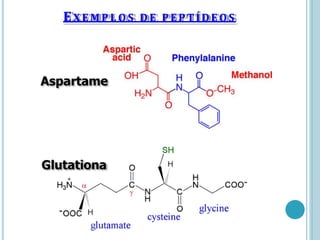
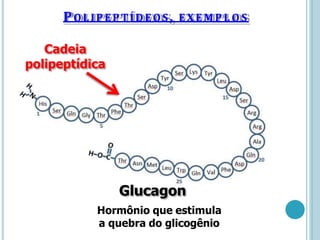
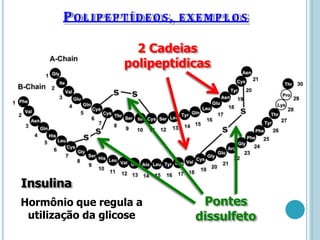
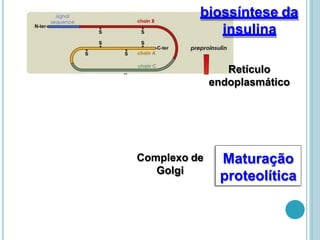
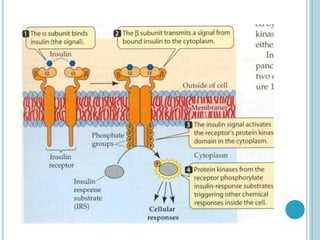
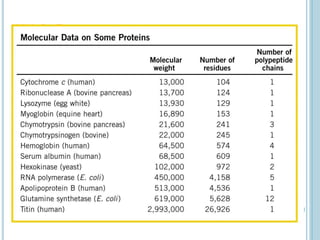
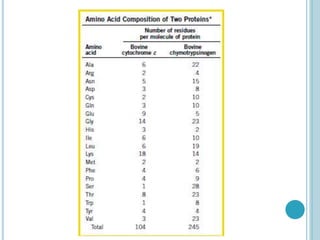
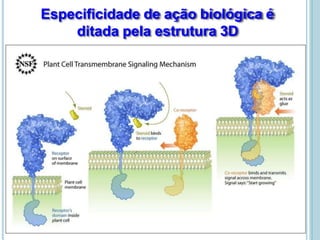
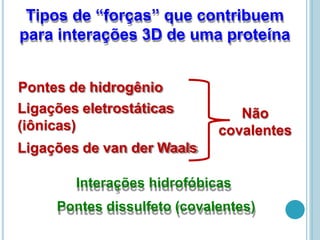
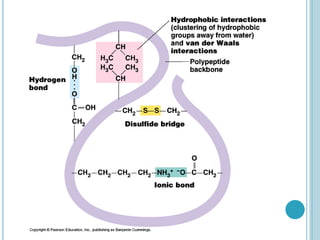
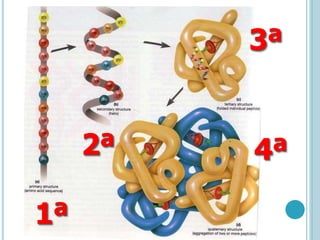
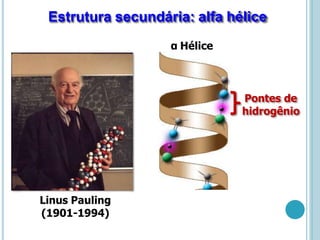
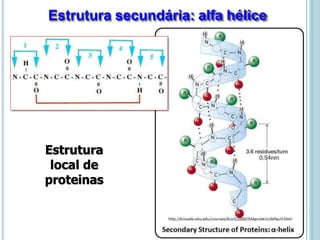
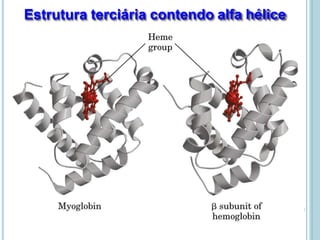
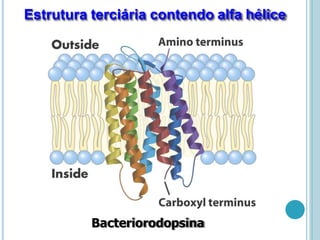
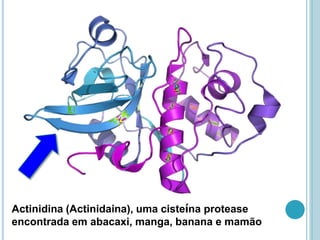
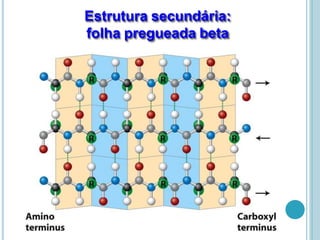
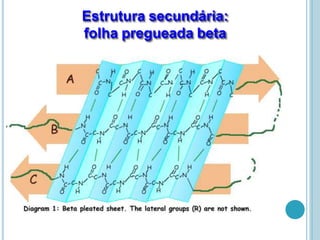
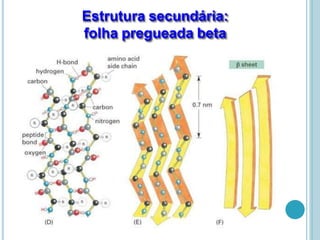
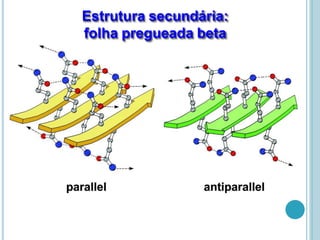
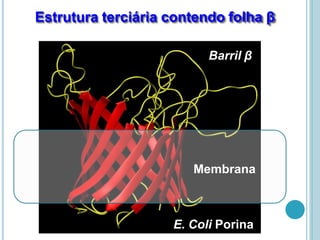
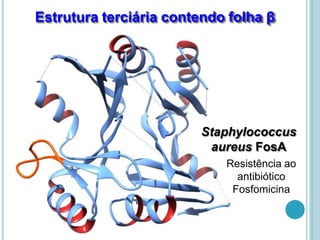
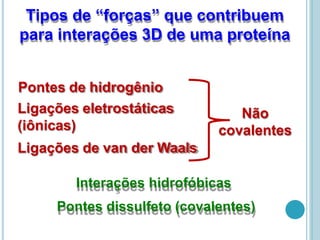
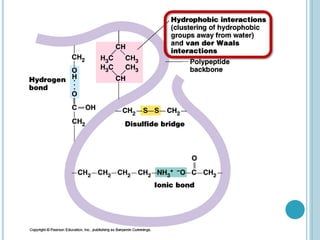
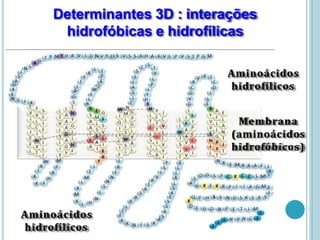
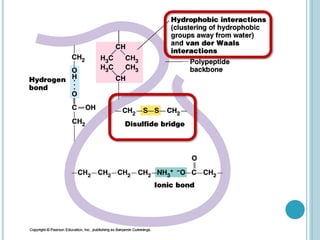
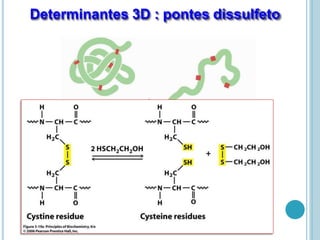
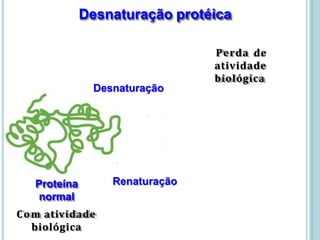
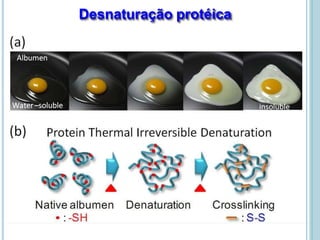
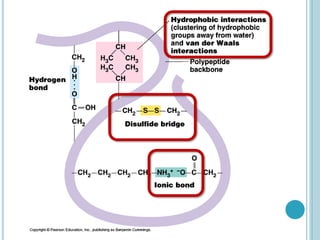
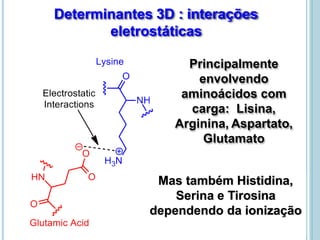
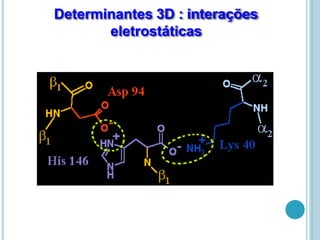
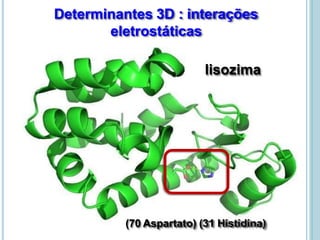
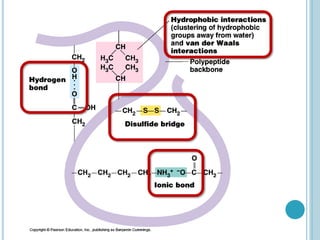
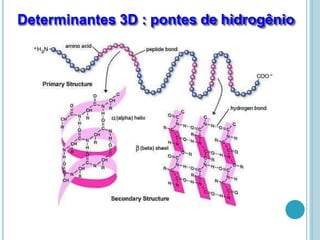
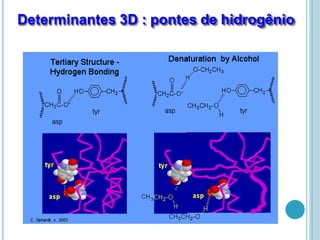
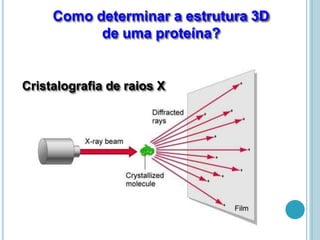
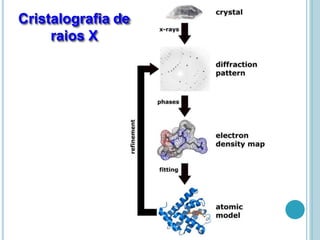
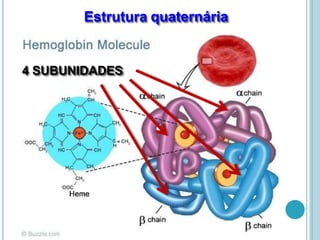
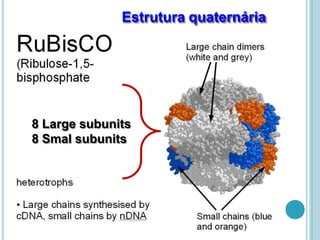
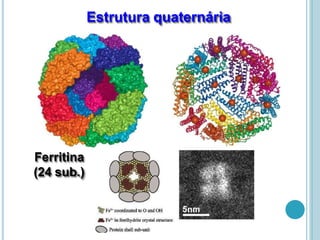
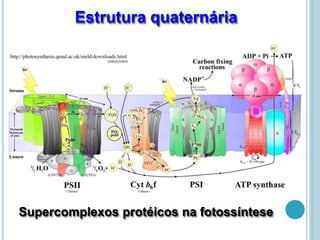
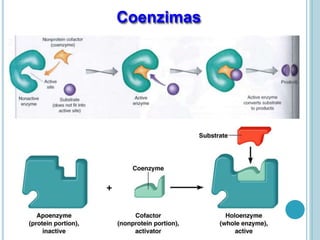
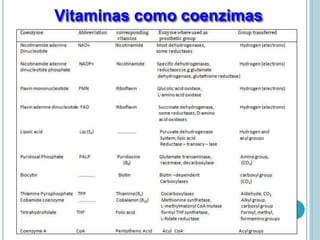
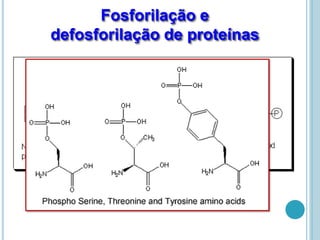
O documento discute a estrutura e função de aminoácidos, peptídeos e proteínas. Aborda a importância das proteínas, sua diversidade de funções, classificação de acordo com as funções e aminoácidos. Explora a composição das proteínas por repetições de aminoácidos e os níveis de estrutura das proteínas.