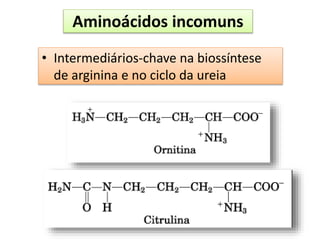
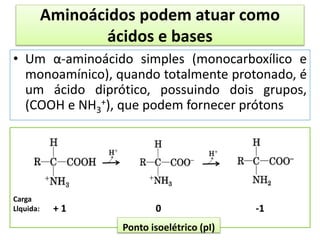
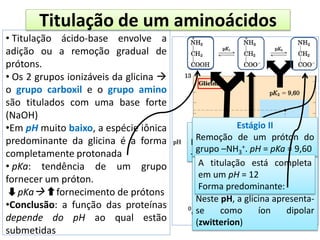
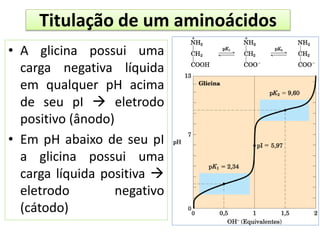
O documento discute os aminoácidos, peptídeos e proteínas, abordando:
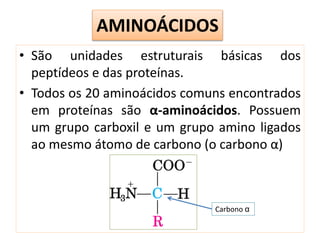
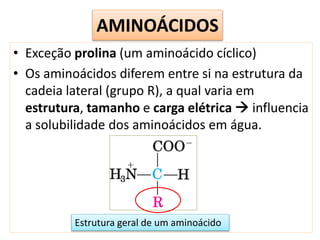
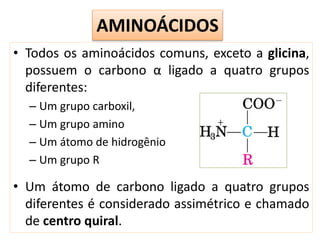
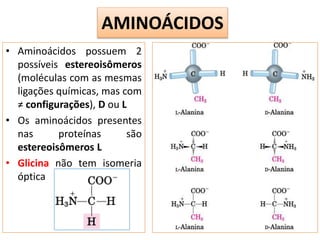
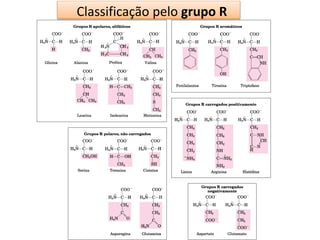
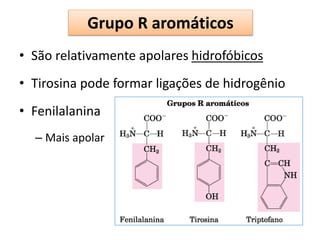
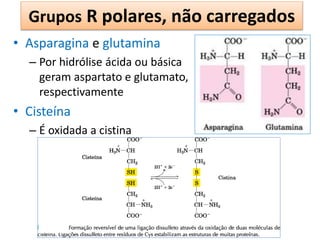
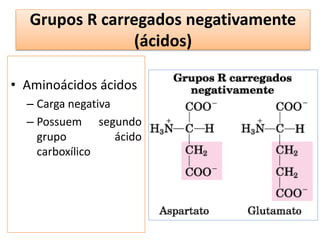
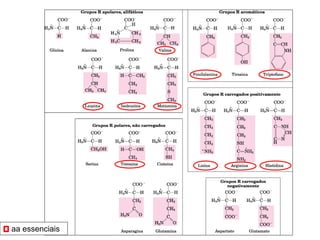
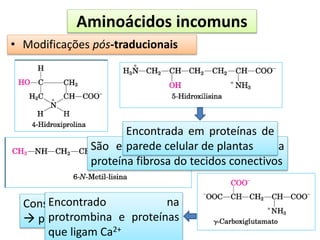
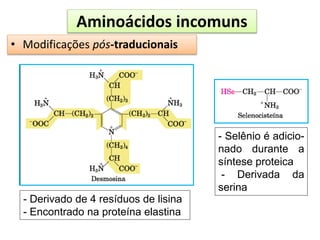
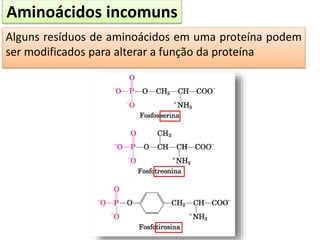
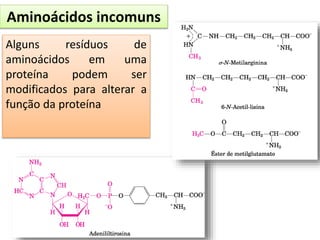
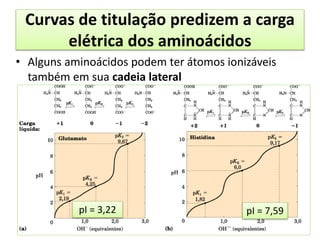
1) As características químicas dos aminoácidos e suas classificações;
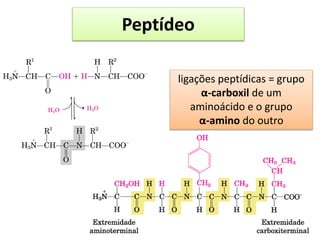
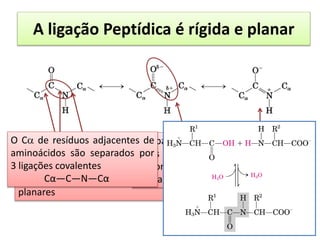
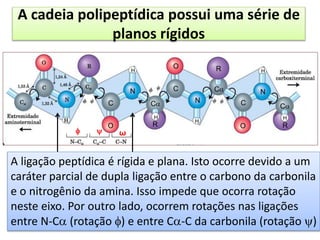
2) A formação de ligações peptídicas na união de aminoácidos em cadeias polipeptídicas;
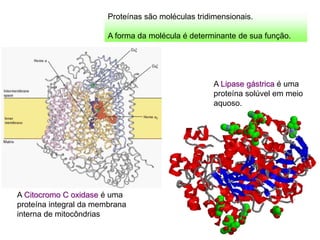
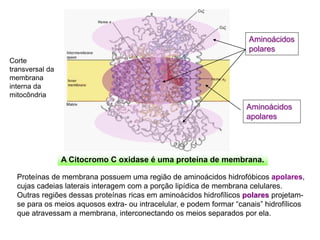
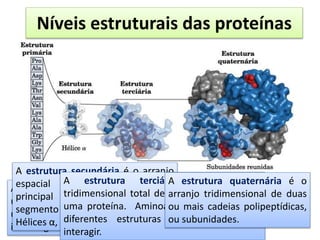
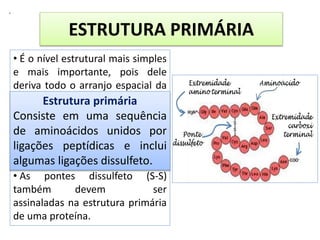
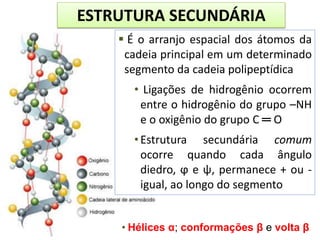
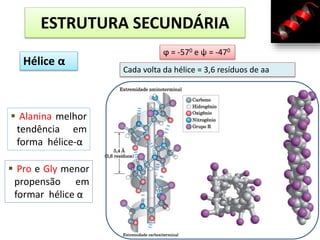
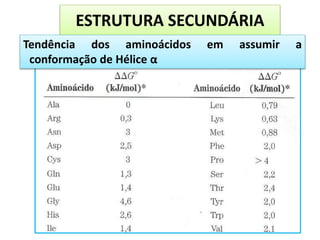
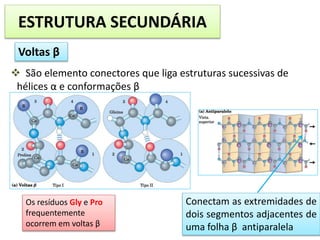
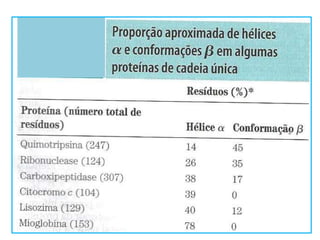
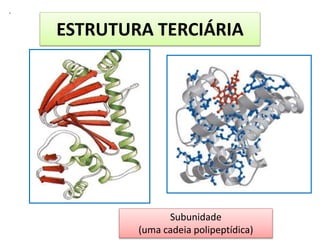
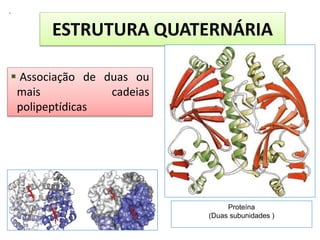
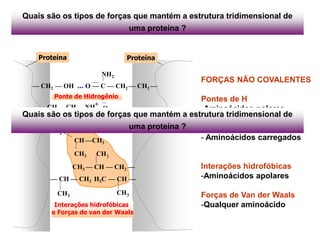
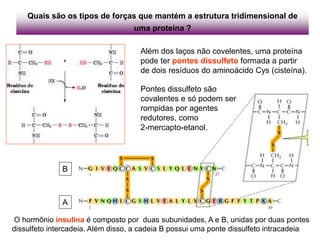
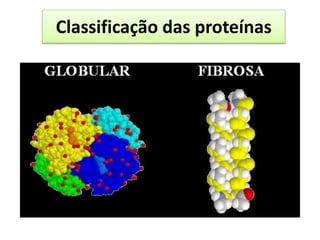
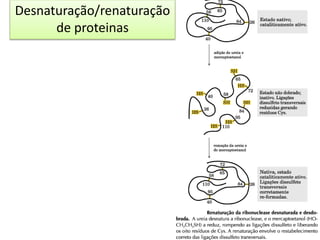
3) Os diferentes níveis estruturais das proteínas, incluindo estrutura primária, secundária, terciária e quaternária.