Aminoácidos: estrutura e classificação
- 1. AMINOÁCIDOS
- 2. O dogma central da Biologia Molecular Uma vez a informação chega à proteína não flui de volta para o DNA.
- 3. Por que estudar proteínas? - As proteínas são as macromoléculas mais abundantes nas células; -Grande variedade de tamanhos e tipos; - Grande variedade de funções biológicas -São os produtos da informação gênica! - São os instrumentos pelos quais a informação gênica é expressa! - Quase todo o trabalho celular é feito por proteínas.
- 4. As proteínas têm estruturas muito variadas
- 5. As proteínas têm funções muito variadas
- 6. As proteínas têm funções muito variadas
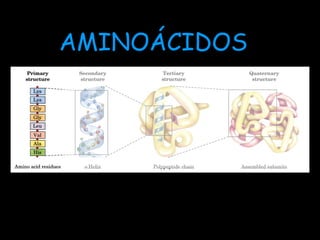
- 7. Níveis estruturais das proteínas
- 9. As proteínas são polímeros de aminoácidos Cada resíduo de aminoácido é ligado ao vizinho por uma ligação covalente, a ligação peptídica
- 10. Estrutura geral dos aminoácidos Todos os aminoácidos comuns são α-aminoácidos Os Aminoácidos apresentam um grupo carboxílico e um grupo amino ligados ao mesmo carbono (carbono α). Estrutura geral: Carbono α - Centro quiral O QUE DIFERE UM AMINOÁCIDO DO OUTRO É O GRUPAMENTO/CADEIA LATERAL!!! Grupamento carboxìl Grupamento amino
- 11. Identificaçãodos carbonos em um aminoácido
- 12. Os aminoácidos têm atividade óptica Virtualmente todos os aminoácidos achados em proteínas são isômeros L
- 13. O que difere um aminoácido do outro é o grupamento (ou cadeia) lateral (R) Os aminoácidos são classificados de acordo com as propriedades de seus grupamentos laterais. A cadeia lateral e a classificação dos aminoácidos Cadeia Lateral – varia em tamanho, estrutura, carga elétrica e influencia a solubilidade do aminoácido em água.
- 14. Classificação dos AminoácidosClassificação dos Aminoácidos Como você classificaria estas latas?
- 15. Conteúdo de açúcar? Cor? Fabricante? Sabor?
- 16. Classificação dos aminoácidos de acordo com a propriedade dos grupos laterais
- 18. Classificação dos aminoácidos: 1 – Aminoácidos com grupamentos laterais apolares e alifáticos
- 19. Cadeias laterais tendem a se agrupar Estabilização da proteína por interação Hidrofóbica não tem contribuição real para Interação Hidrofóbica estrutura cíclica/conformação rígida/ reduz a flexibilidadegrupo tioeter não polar Sobre os aminoácidos com grupamentos laterais apolares e alifáticos:
- 20. Classificação dos aminoácidos: 2 – Aminoácidos com grupamentos laterais aromáticos • relativamente não polares (hidrofóbicas) • participam em interações hidrofóbicas. • grupo OH da tirosina – pode formar ponte de hidrogênio – grupo funcional importante em algumas enzimas • Tirosina e Triptofano – mais polares do que Fenilalanina
- 22. Classificação dos aminoácidos: 3 – Aminoácidos com grupamentos laterais polares não carregados Grupos R – mais solúveis em água ou mais hidrofílicos do que os não polares – grupos funcionais que formam ligações de hidrogênio com a água. Exceto cisteína Polaridade conferida por: • Serina e Treonina –hidroxila • Cisteína – sulfidrila • Asparagina e glutamina - amida
- 23. Formação de Cistina Dois resíduos de Cisteína se oxidam e formam o aminoácido dimérico Cistina Ponte dissulfeto
- 24. Classificação dos aminoácidos: 4 – Aminoácidos com grupamentos laterais carregados positivamente • Lisina – 2o grupo amino na posição ε • Arginina – grupo guanidino • Histidina – grupo imidazol (pKa ~neutro) – doador/receptor de protons em muitas reações enzimáticas – fração significante carregada positivamente em pH neutro Grupo R – carga positiva em pH 7,0
- 25. Classificação dos aminoácidos: 5 – Aminoácidos com grupamentos laterais carregados negativamente Aspartato e Glutamato segundo grupo carboxila Grupo R – carga negativa em pH 7,0
- 26. Os grupamentos laterais polares e carregados tendem a mapear na superfície da proteína Diagrama de Ribbon Mapa de superfície
- 27. Os grupamentos laterais não polares tendem a se enterrar no centro das proteínas Grupamentos laterais não polares heme Mioglobina
- 28. Os aminoácidos podem agir como ácidos e como bases
- 29. Dissociação dos AminoácidosDissociação dos Aminoácidos COOCOO-- CHCH33 H-C-NHH-C-NH33 ++ H-C-NHH-C-NH22 COOCOO-- CHCH33 COOHCOOH CHCH33 H-C - NHH-C - NH33 ++ pKpK11 pKpK22 Região de tamponamento devida ao grupo -COOH Base- capta prótons do meio Ácido -doa prótons para o meio Região de tamponamento devida ao grupo -NH2
- 30. Derivados de aminoácidos com atividade biológica
- 31. • pH neutro – íons dipolares ou “zwitterions” grupo α-amino – protonado (íon amônio – NH3 + ) grupo α-carboxila – dissociado (íon carboxilato – COO- ) • opticamente ativos – desviam o plano da luz polarizada carbono α – centro quiral – ligado a quatro substituintes diferentes arranjados em configuração tetraédrica e assimétrica Estereoisômeros – moléculas que diferem somente no arranjo espacial • α- aminoácidos – configuração estereoquímica L Por convenção – forma L – grupo α-NH3 + - projetado para a esquerda forma D – grupo α-NH3 + - projetado para a direita • Cadeia lateral (R) – determina as propriedades físico-químicas de cada aminoácido Características comuns dos aminoácidos