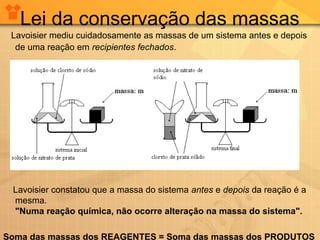
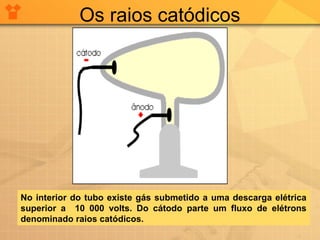
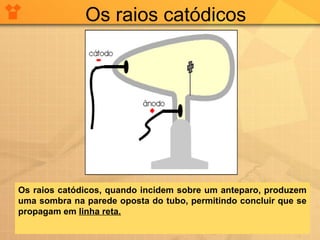
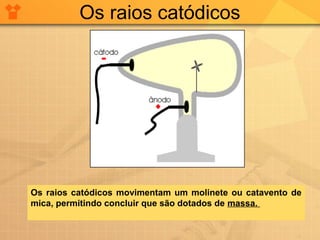
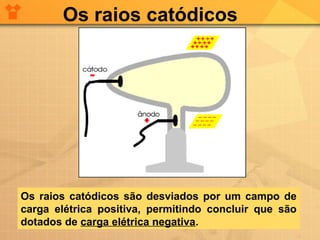
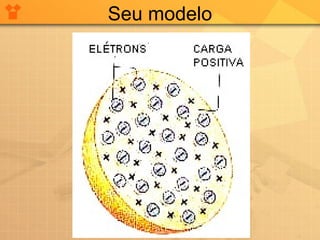
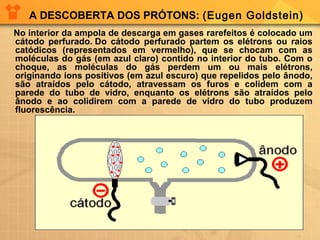
O documento descreve a evolução das teorias atômicas desde a Antiguidade até o modelo de Thomson. Inicialmente, Leucipo e Demócrito formularam a teoria de que a matéria é constituída por átomos indivisíveis. Aristóteles rejeitou esta teoria. Posteriormente, Dalton propôs que cada elemento químico é constituído por um único tipo de átomo. Thomson realizou experimentos que mostraram que os átomos continham partículas ainda menores, os elétrons, com carga negativa.