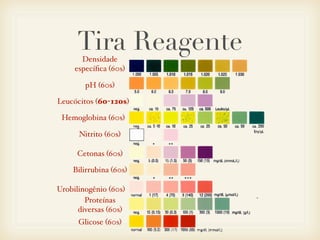
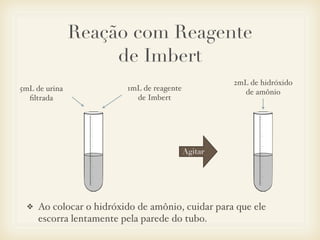
O documento resume os principais procedimentos e testes realizados em uma urinálise, incluindo a coleta de amostras de urina, medição de volume, densidade, pH e testes para detecção de glicose, proteínas, hemoglobina e outros componentes usando tiras reagentes ou reações químicas como as de Benedict e Heller.