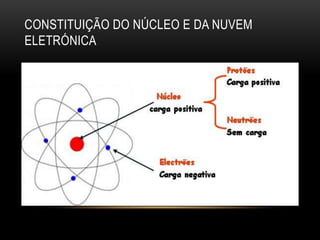
O documento descreve a constituição dos átomos. Um átomo é a menor partícula de um elemento químico e é constituído por prótons, nêutrons e elétrons. Os prótons e nêutrons formam o núcleo no centro do átomo e os elétrons giram em sua volta. O número de prótons define qual elemento químico é, enquanto o número total de prótons e nêutrons determina o isótopo específico.