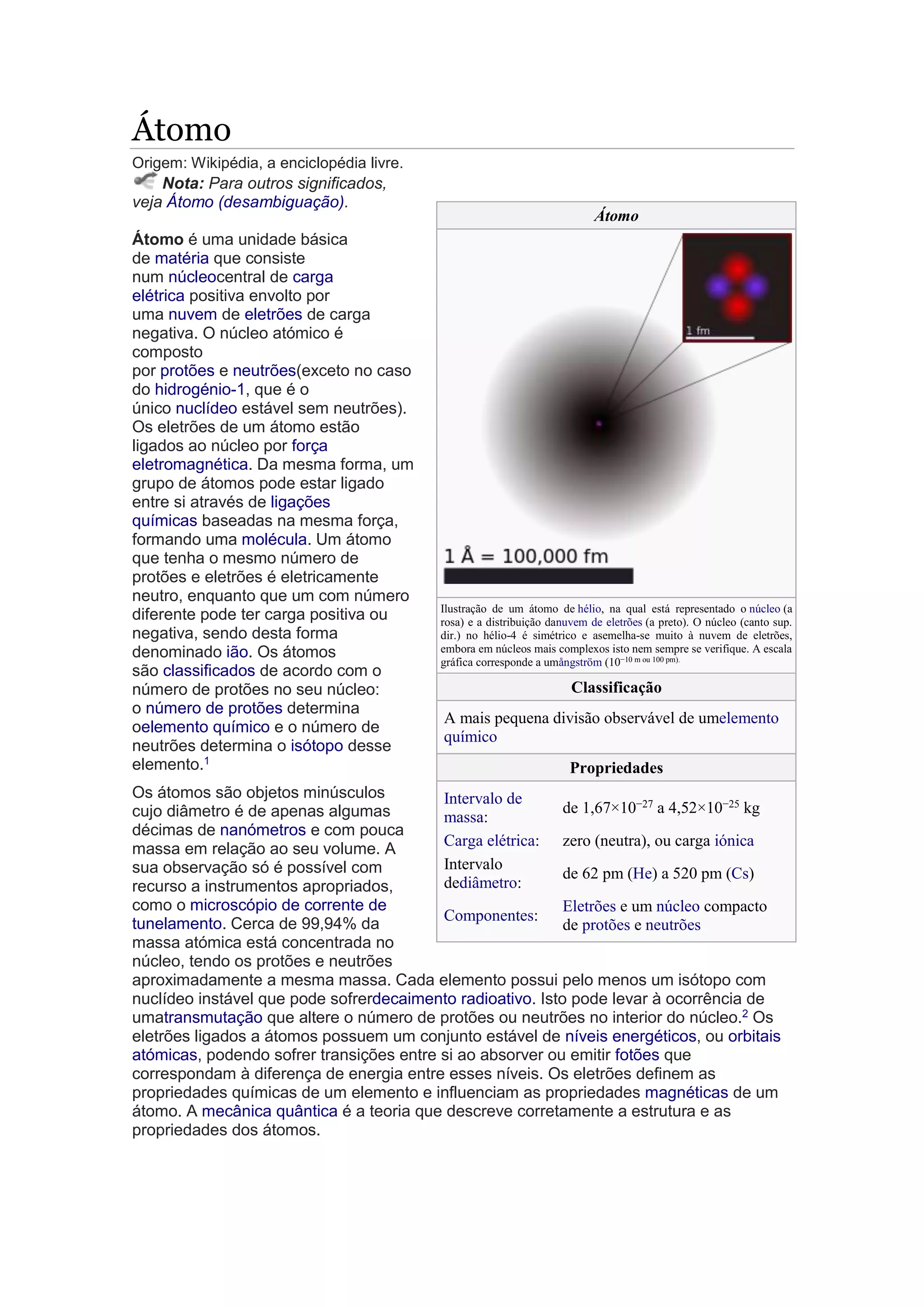
1) Um átomo é a menor unidade de matéria que consiste em um núcleo central positivo rodeado por eletrões negativos.
2) O núcleo é composto de prótons e nêutrons, e os eletrões são atraídos por força eletromagnética.
3) Átomos são classificados pelo número de prótons, que determina o elemento químico, enquanto o número de nêutrons determina o isótopo.