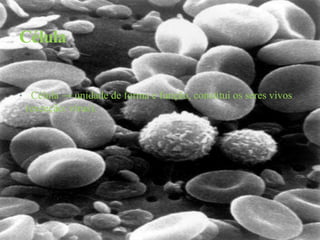
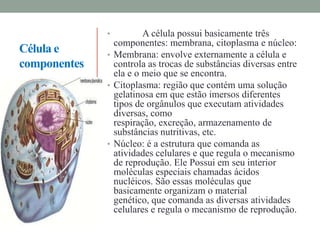
1) O documento propõe um trabalho sobre conceitos-chave da biologia celular como átomo, molécula, célula, órgão e indivíduo.
2) Deve-se explicar a relação entre células e órgãos e comparar as células e órgãos de seres animais e vegetais.
3) O trabalho deve ser apresentado em PowerPoint com um glossário contendo imagens e explicações dos conceitos.









![Exemplos
• Dois átomos de
hidrogénio se combinam
para formar uma
molécula de
hidrogénio oxigénio [O2
].
• Um átomo de oxigénio
se combina com dois
átomos de hidrogénio
para formar a molécula
de água [H2O].](https://image.slidesharecdn.com/apresentao1-1trabalho-paracd-111220114354-phpapp02/85/Apresentacao1-1-trabalho-para-cd-13-320.jpg)