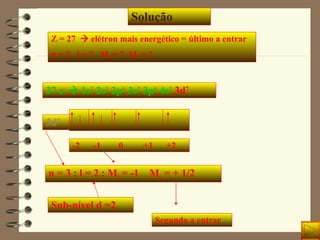
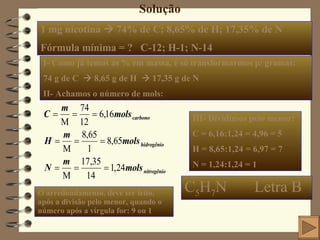
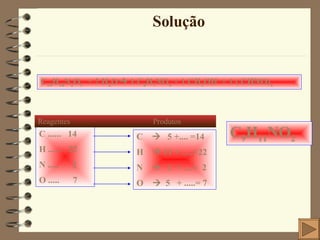
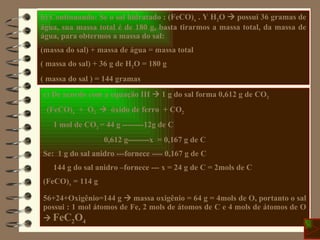
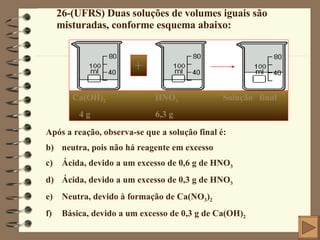
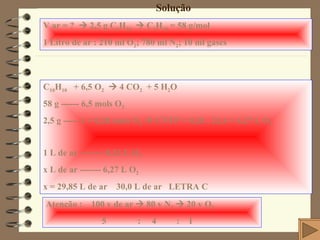
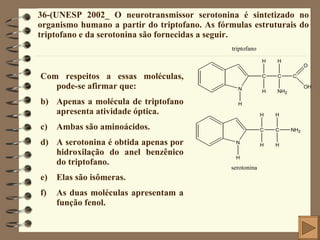
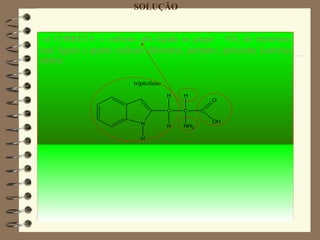
O documento apresenta 15 questões sobre química inorgânica e orgânica. As questões abordam tópicos como: distribuição eletrônica de átomos e íons; cálculo de massa atômica; geometria molecular; ligação química em compostos iônicos e moleculares; polaridade de moléculas; e estrutura eletrônica de elementos químicos.