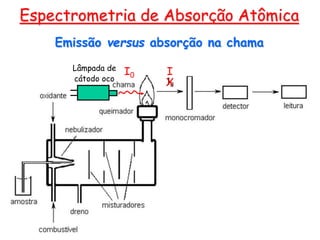
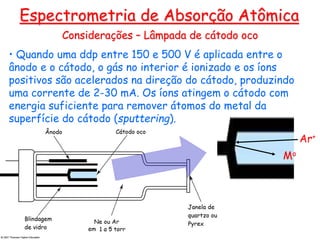
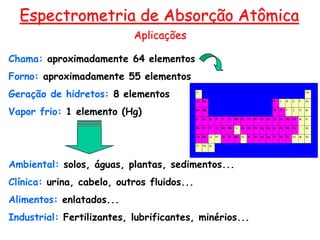
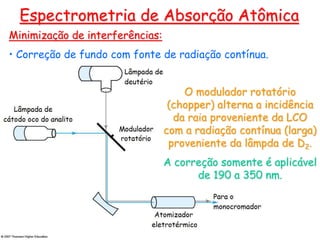
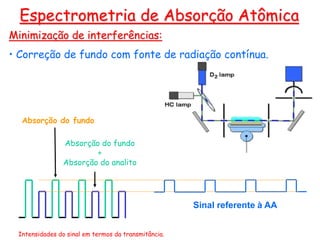
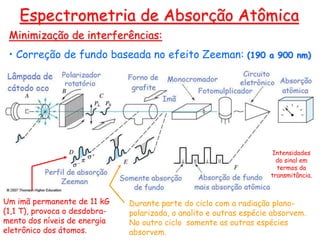
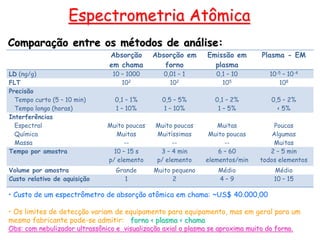
O documento resume os principais conceitos e técnicas da espectrometria de absorção atômica, incluindo: (1) a descrição da técnica e sua aplicação na análise de metais; (2) os componentes principais como fonte de radiação, sistemas de atomização, e detectores; e (3) formas de minimizar interferências no processo analítico.