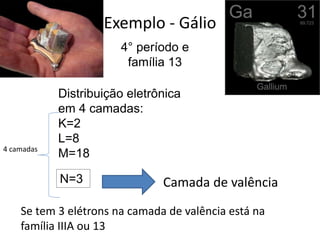
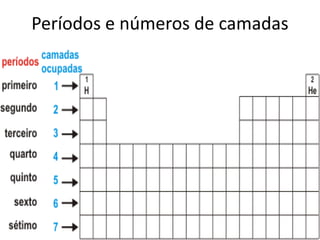
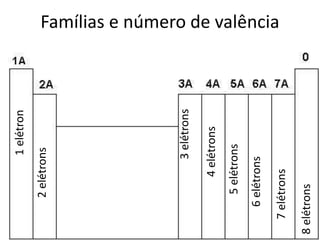
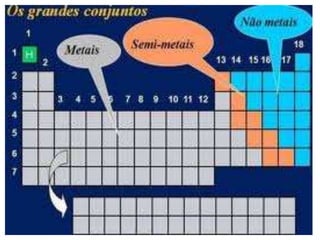
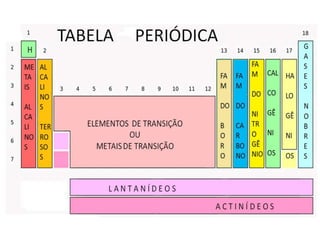
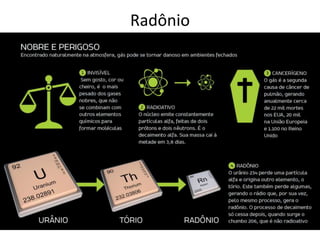
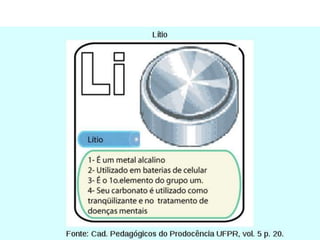
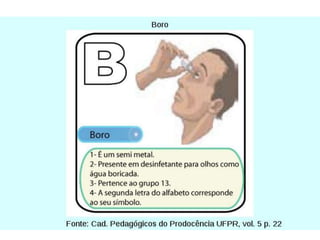
O documento descreve a tabela periódica, incluindo sua organização de acordo com o número atômico e massa, propriedades periódicas dos elementos, distribuição eletrônica, períodos e famílias. Explica as características dos metais, semimetais, ametais e gases nobres. Por fim, pede uma pesquisa sobre poluentes tóxicos que ameaçam o planeta.