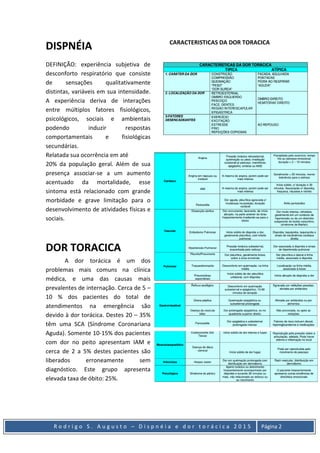
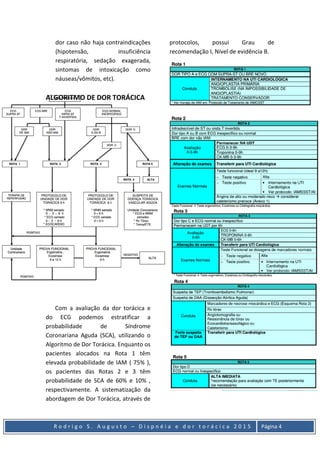
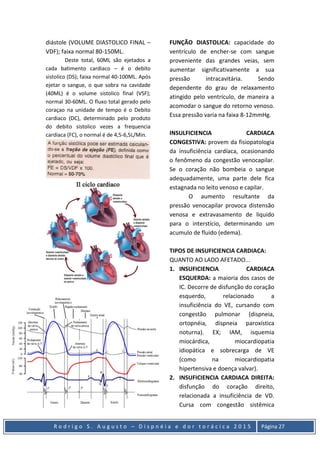
O documento discute dispneia e dor torácica, definindo dispneia como uma experiência subjetiva de desconforto respiratório e listando fatores que contribuem para a dor torácica. Também descreve síndrome coronariana aguda, embolia pulmonar e marcadores de necrose miocárdica, incluindo métodos de diagnóstico e tratamento.