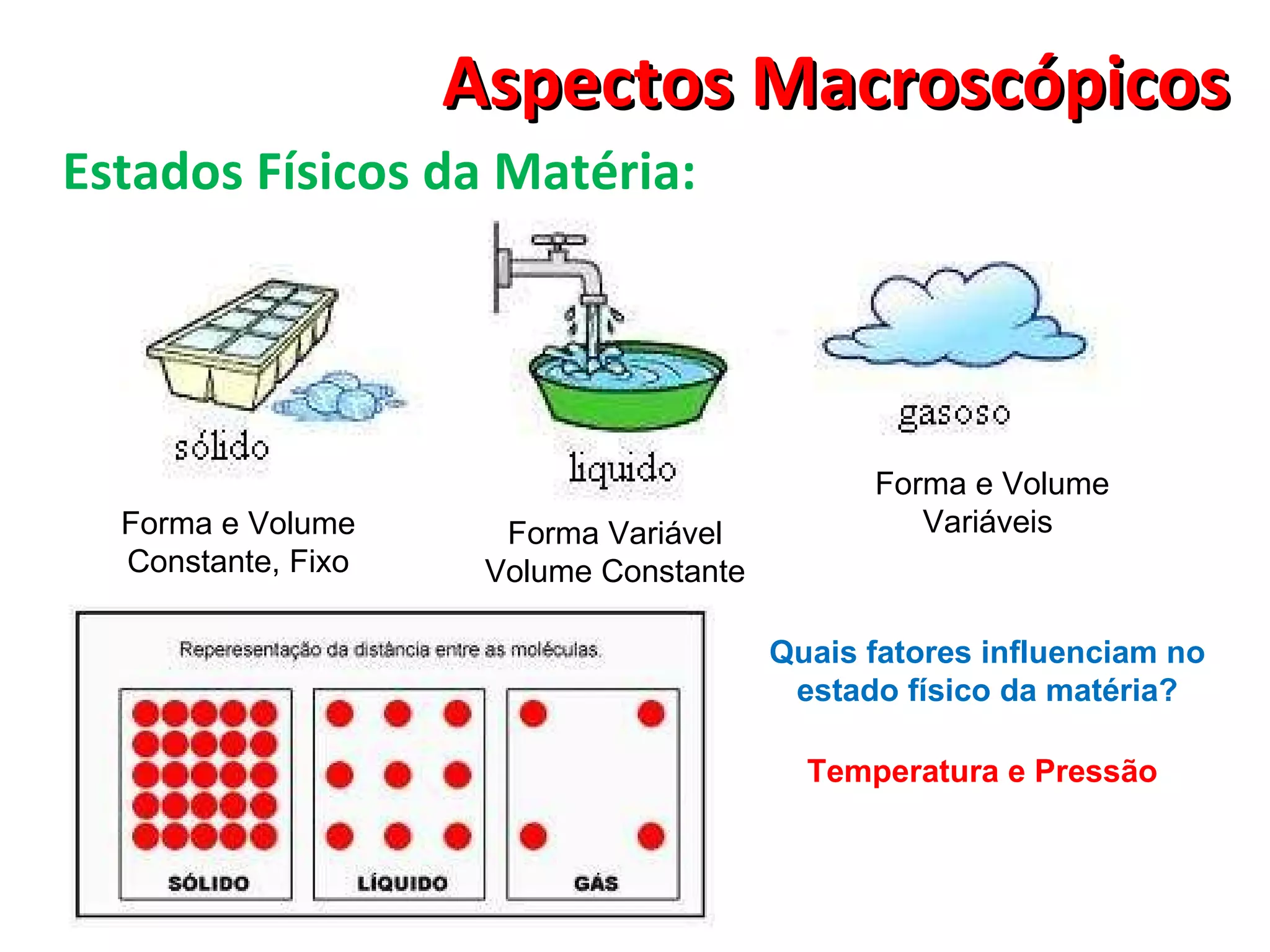
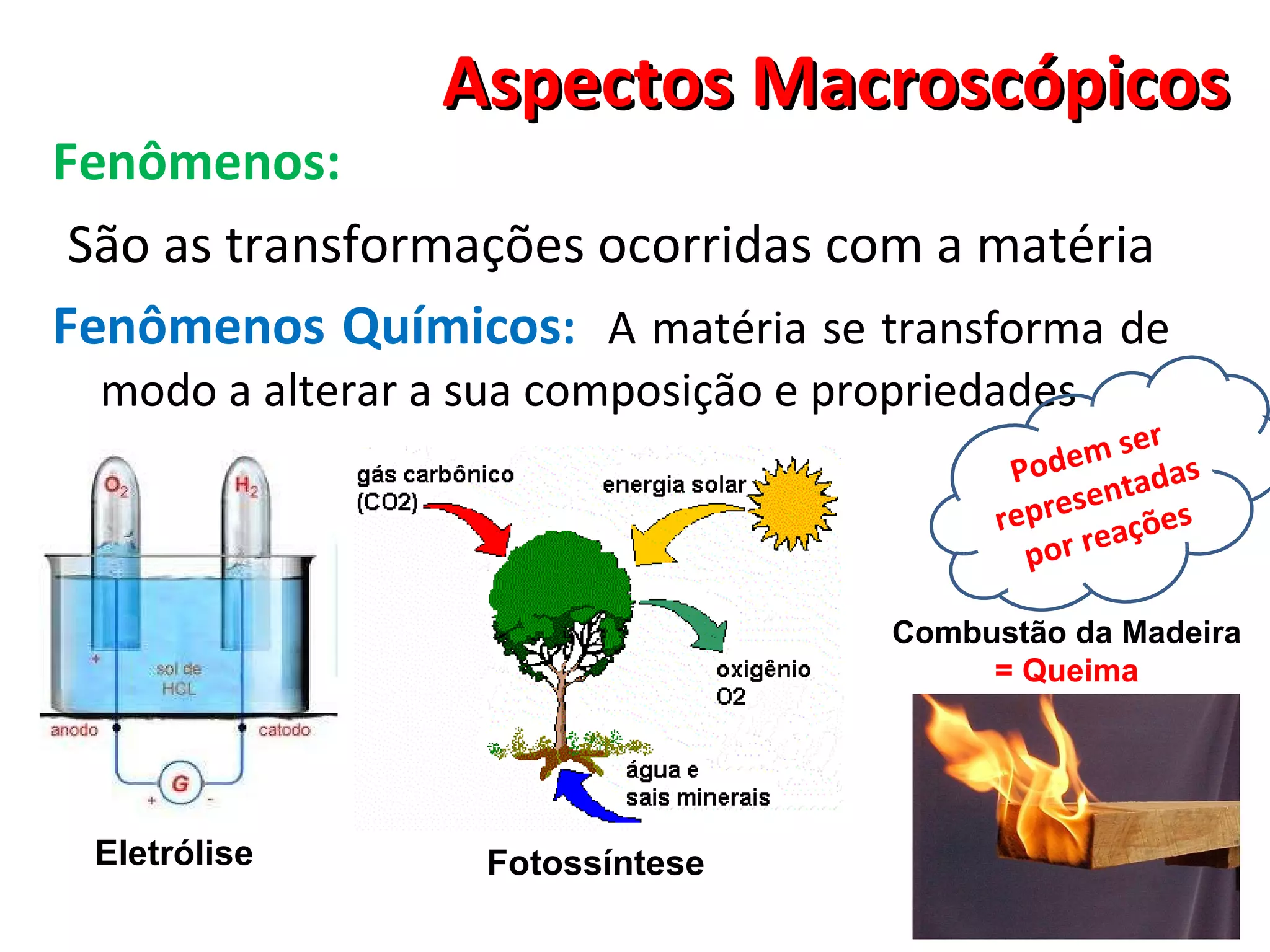
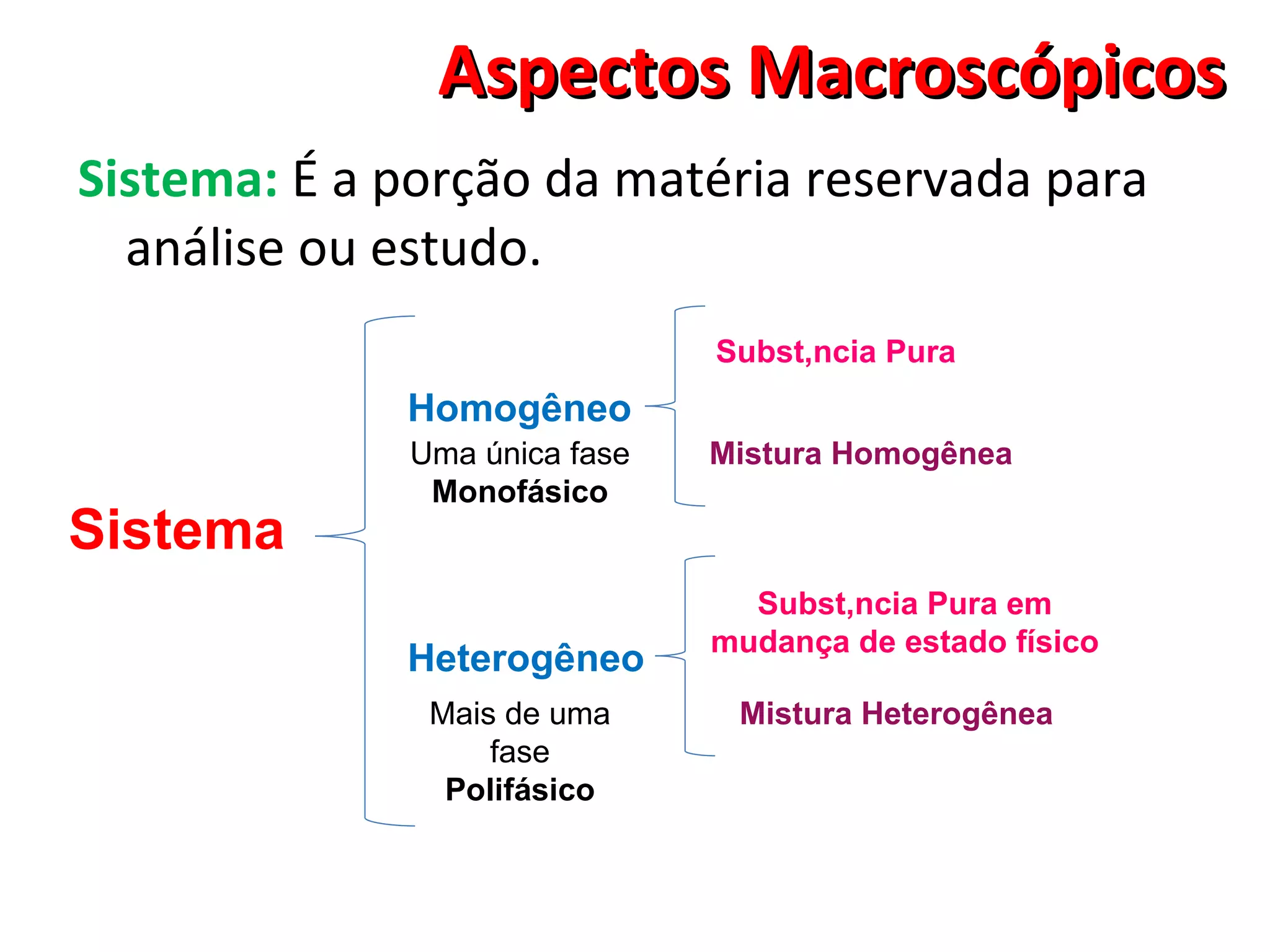
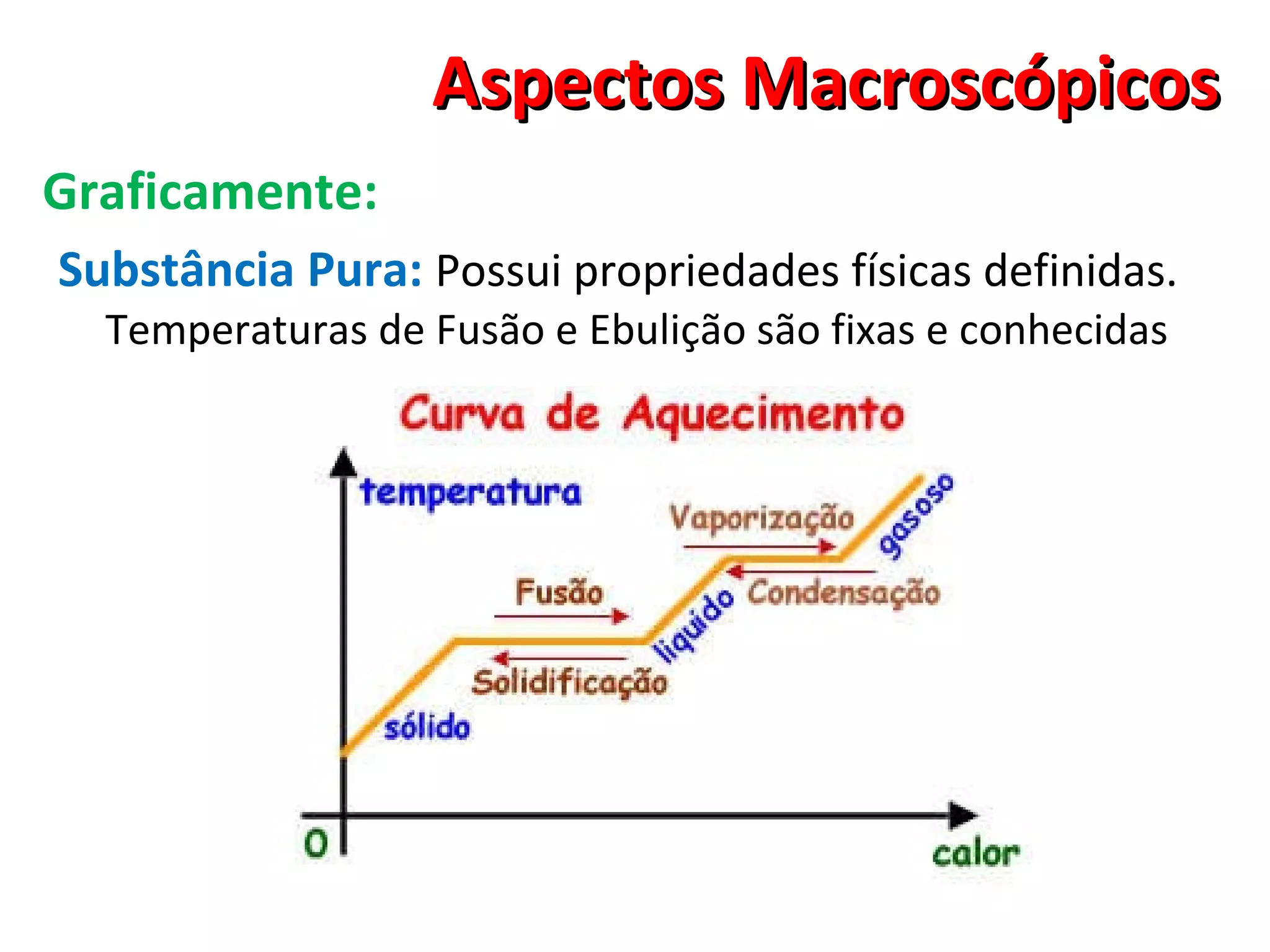
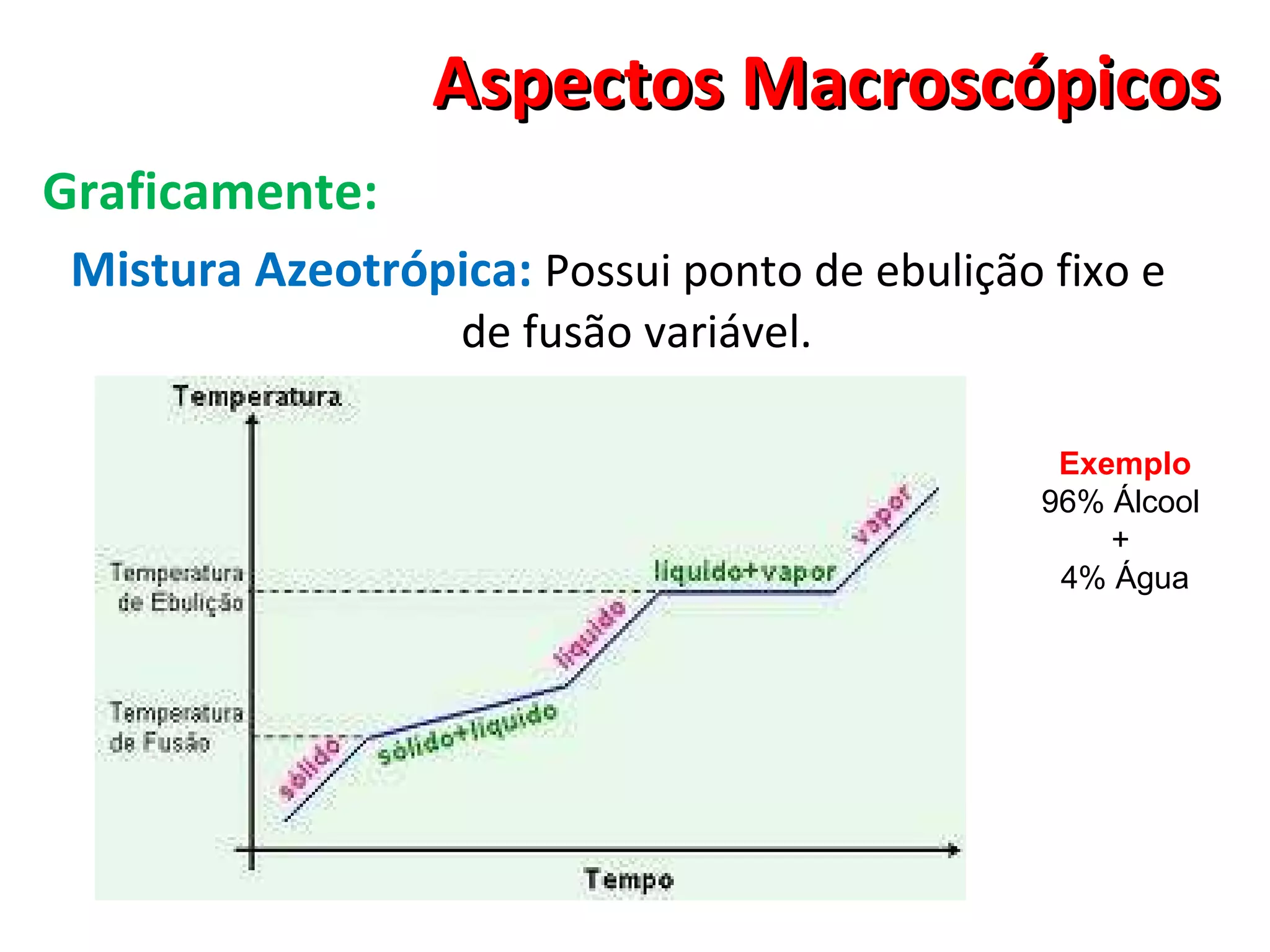
O documento discute conceitos macroscópicos da matéria, incluindo que a matéria pode existir em diferentes estados físicos e que fatores como temperatura e pressão influenciam essas mudanças de estado. Também aborda conceitos como corpos, objetos, propriedades da matéria, alotropia, misturas e sistemas.