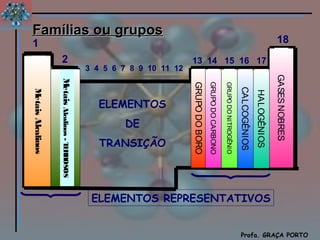
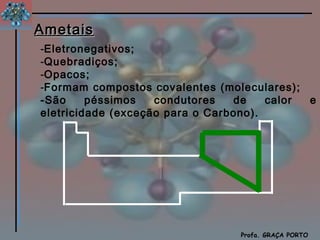
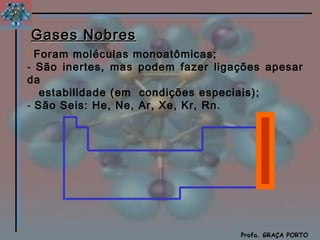
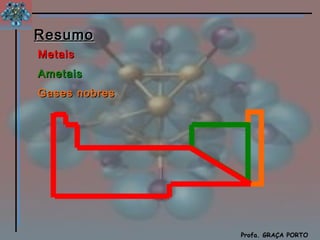
O documento descreve a história da tabela periódica, incluindo as contribuições de Döbereiner, Newlands e Mendeleiev. Explica a organização dos elementos de acordo com seus números atômicos em períodos e grupos, e as propriedades dos metais, ametais e gases nobres.