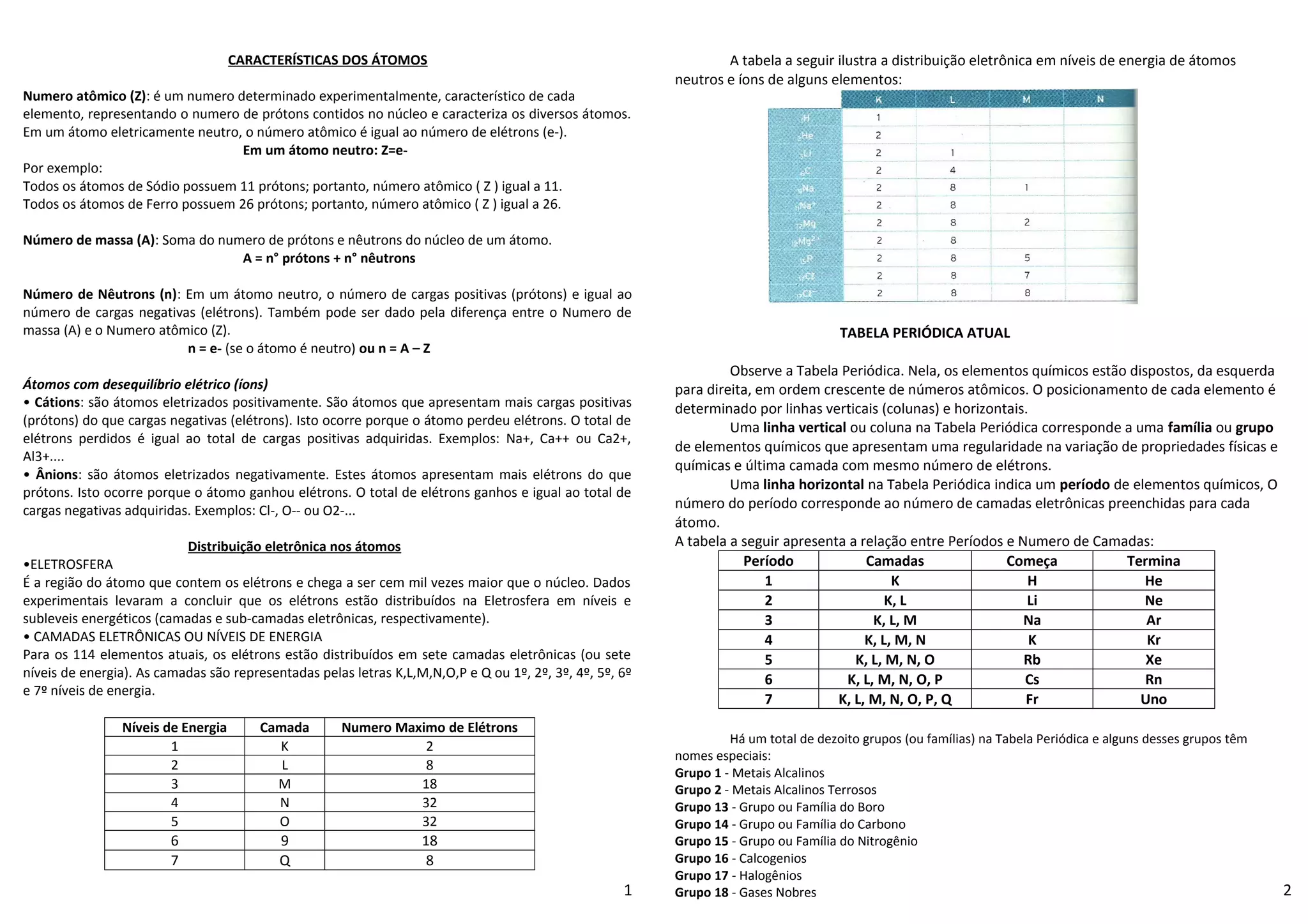
1) O documento descreve as características dos átomos, incluindo o número atômico, número de massa, distribuição eletrônica e tipos de ligações químicas.
2) Os átomos são caracterizados pelo número atômico e número de massa. Os elétrons são distribuídos em camadas eletrônicas com diferentes níveis de energia.
3) Existem três tipos principais de ligações químicas: iônica, covalente e metálica, dependendo da distribuição eletrô