7 titulacoes
- 2. Os ácidos e as bases fortes estão completamente ionizados/ dissociados em solução aquosa. Assim pode-se escrever: )(2)()()( laqaqaq OHNaClNaOHHCl )()()( aqaqaq OHNaNaOH A mistura de HCl e NaOH, pode ser traduzida pela equação química: )(2)()()()()(3)( 2 laqaqaqaqaqaq OHNaClOHNaOHCl Como se observa, há partículas que: • efetivamente reagem , H3O+ e OH-; • são apenas iões espetadores , Cl- e Na+. A reação inversa da autoionização da água é muito extensa )(3)()(2)( aqaqlaq OHClOHHCl Equação geral: TITULAÇÃO ÁCIDO-BASE
- 3. Titulação ácido-base (volumetria ácido-base) – permite determinar a concentração desconhecida de um ácido (uma base) numa solução – titulado – fazendo reagir essa solução com uma base (um ácido) de concentração conhecida – titulante. Titulante Titulado TITULAÇÃO ÁCIDO-BASE
- 5. Numa titulação ácido-base adiciona-se titulante ao titulado até se atingir o ponto de equivalência. Momento em que ambos reagem estequiometricamente: nácido = nbase cácido Vácido = cbase Vbase Apenas válido para estequiometria monoácido/monobase (1: 1). Como sabemos que se atingiu o ponto de equivalência? -No ponto de equivalência verifica-se uma variação brusca do pH -Pode ser detetado utilizando um indicador de ácido-base adequado, adicionado ao titulado. Este muda de cor no ponto de equivalência. - Na realidade o que é detetado é o ponto final – momento em que o ponto de equivalência é ultrapassado. - Se o indicador for bem escolhido, o ponto de equivalência e o ponto final são próximos. TITULAÇÃO ÁCIDO-BASE
- 6. Como se processa uma titulação volumétrica? 1º - Coloca-se na bureta determinado volume de uma solução de concentração conhecida com rigor – Titulante. 2º - Coloca-se no erlenmeyer um volume conhecido da solução de concentração a determinar – Titulado. V - ? C - Conhecida V - Conhecido C - ?
- 7. Como se processa? 3º -Mede-se o volume inicial de titulante - Vi 4º -Adiciona-se aos poucos o titulante à solução (titulado) no erlenmeyer.
- 8. O ponto final é detetado pela variação de uma propriedade física ou química da solução a ser titulada, utilizando indicadores o instrumentalmente. Quando se utilizam os indicadores, esta variação é facilmente detetada, pois corresponde a uma alteração de cor. Como se processa? 5º -O titulante é adicionado ao titulado até que se atinja a quantidade estequiométrica. A titulação termina quando se atinge o ponto final da reacção ou ponto de equivalência da reacção.
- 9. 6º -Mede-se o volume final de titulante - Vf Como se processa? 7º -Determina-se o volume de titulante utilizado Vtitulante= Vf - Vi
- 10. O ponto estequiométrico, de equivalência ou final teórico de uma titulação é aquele calculado com base na estequiometria da reação envolvida na titulação. O ponto final de uma titulação é aquele determinado experimentalmente. Numa titulação ideal, o ponto de equivalência coincidiria com o ponto final da titulação. Na prática, há sempre uma pequena diferença, que constitui o chamado erro de titulação. Ponto de equivalência ou ponto final
- 11. Determinação do ponto final de uma titulação. Indicadores visuais: Causam mudança de cor próximo do ponto de equivalência. Métodos instrumentais: Medida de pH, condutividade, potencial, corrente, temperatura, etc.
- 12. Condições a que devem obedecer as reações utilizadas em volumetria: Uma reacção química a utilizar em volumetria deve ser: estequiométrica, rápida; completa; possibilitar a de deteção do ponto de equivalência.
- 13. Estequiométrica, rápida, completa e com um ponto de equivalência detetável. • A reação deve ser estequiométrica, isto é, deve ser expressa por uma equação química, bem conhecida. • Deve ser rápida, para permitir atingir eficazmente o ponto de equivalência. No caso de a reação ser lenta, e continuando a ser feita a adição de solução titulante, o ponto de equivalência será atingido com um excesso de volume de solução.
- 14. Estequiométrica, rápida, completa e com um ponto de equivalência detetável. A reacção tem de ser completa, e não podem ocorrer reacções secundárias, caso contrário é impossível o cálculo do resultado da análise. Deve possibilitar a de deteção do ponto de equivalência por visualização da alteração repentina de uma propriedade da solução (pH, temperatura, condutividade). Para auxiliar a deteção do ponto de equivalência, podem ser utilizados, indicadores visuais ou métodos instrumentais.
- 15. Titulante – Solução Padrão Para ser possível determinar com rigor a concentração da solução a titular, o titulante deve ser uma solução padrão, ou seja, uma solução cuja concentração seja rigorosamente conhecida. Este tipo de soluções são preparadas a partir das suas substâncias primárias.
- 16. Como escolher o indicador? Teremos que saber o ponto de equivalência, através da curva de titulação. Curvas de Titulação O indicador adequado é aquele cuja zona de viragem contém o ponto de equivalência. Mas tem de ser Um indicador cuja zona de viragem esteja contida na zona abrupta da curva. TITULAÇÃO ÁCIDO-BASE
- 17. Curvas de Titulação TITULAÇÃO ÁCIDO-BASE
- 18. pH inicial do titulado (base) Próximo do ponto de equivalência há uma variação brusca do pH: (de 11 para 3,6) Ponto de equivalência (zona de inflexão) Volume de titulante (ácido) gasto para atingir o ponto de equivalência TITULAÇÃO ÁCIDO-BASE
- 20. EXERCÍCIO Observe a seguinte figura e determine a concentração de HCl desconhecida, presente no titulado. R: [NaOH]= 0,1 mol dm-3 VNaOH gasto = 10 mL = 0,01dm3 [HCl]= ? mol dm-3 VHCl = 25 mL = 0,025 dm3 Como estequiometria 1: 1 na= nb Ca Va = Cb Vb Ca 0,025 = 0,1 0,01 Ca = 0,04 mol dm-3 )(2)()()( laqaqaq OHNaClNaOHHCl
- 21. EXERCÍCIO Na titulação de 20,00 cm3 de uma solução de HNO3, gastaram-se 10,00 cm3 de NaOH de concentração 0,10 mol dm-3. a) Completa a equação química que traduz esta titulação ácido-base. b) Calcule a concentração da solução ácida. c) Qual o pH no ponto de equivalência? Justifique. d) Qual o pH da solução após a adição de 4, 00 cm3 de solução de NaOH? (___)(___))()(3 ___________ aqaq NaOHHNO
- 22. EXERCÍCIO R: a) b) Estequiometria 1:1. Resultado: Ca= 0,05 mol dm-3 c) O pH no ponto de equivalência é 7 (a 25 ºC). No ponto de equivalência existe a solução de um sal derivado de um ácido forte e de uma base forte. Como os iões deste sal não sofrem hidrólise, a solução é neutra. d) nb = cb Vb nb = 0,10 4,00 10-3 nb = 4,00 10-4 mol na = ca Va na = 0,05 20,00 10-3 nb = 10 10-4 mol Nesta altura existe excesso de ácido forte de 6 10-4 mol num volume de 24,00 cm3. A sua concentração é 0,025 mol dm-3. Calculo do pH da solução de HNO3, 0,025 mol dm-3. [H3O+]= [HNO3] ionizado= 0,025 mol dm-3 pH = - log [H3O+]= - log (0,025) pH = 1,6 )(2)(3)()(3 laqaqaq OHNaNONaOHHNO
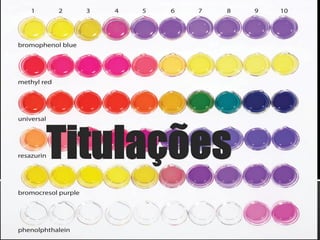
- 25. Existem alguns ácidos fracos que possuem uma certa cor quando na sua forma molecular e uma cor diferente quando estão na forma ionizada. Isso pode ser muito útil, pois dependendo da cor da solução podemos saber se o ácido está ionizado ou não. Mais do que isso, podemos saber a concentração do ião H+ na solução. Por isso dizemos que esses ácidos fracos são indicadores da concentração do ião H+ . Podemos chamar essas substâncias de Indicadores. INDICADORES ÁCIDO-BASE
