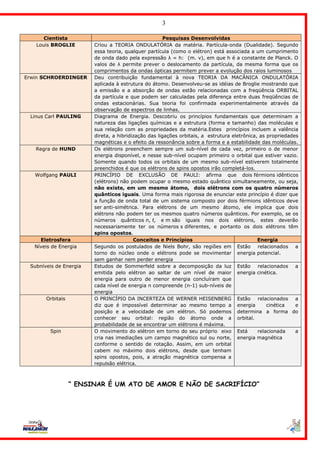
O documento resume a evolução dos modelos atômicos ao longo do tempo, começando pelas ideias de Demócrito e Leucipo sobre átomos indivisíveis. Apresenta os modelos de Dalton, Thomson, Rutherford, Bohr e Sommerfeld, e como as descobertas da física quântica levaram ao desenvolvimento do modelo atômico moderno baseado em orbitais eletrônicos.