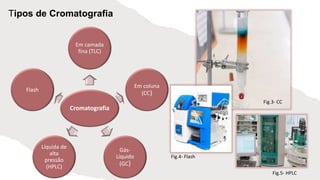
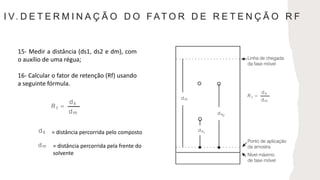
Este documento descreve o procedimento experimental para identificar analgésicos através da cromatografia em camada fina. O método envolve preparar a amostra, aplicá-la na placa junto com padrões, desenvolver o cromatograma, calcular os fatores de retenção e compará-los para identificar os componentes da amostra. A técnica permitiu separar e identificar aspirina em uma amostra, demonstrando a utilidade da cromatografia em camada fina.