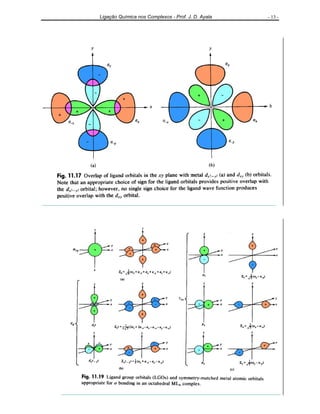
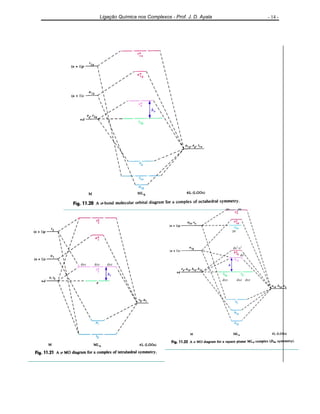
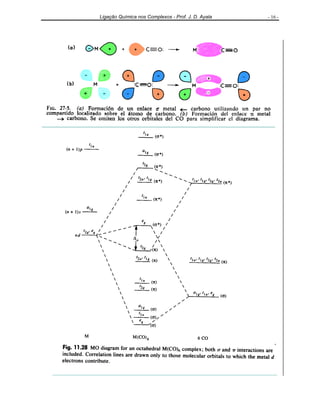
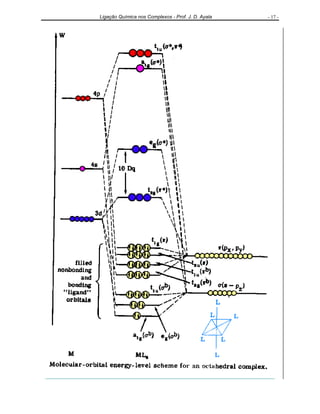
O documento discute as teorias da ligação química em complexos de metais de transição, incluindo a Teoria da Ligação de Valência, a Teoria do Campo Cristalino e a Teoria dos Orbitais Moleculares. Apresenta exemplos de complexos com diferentes geometrias e propriedades magnéticas para ilustrar os conceitos.


![Ligação Química nos Complexos - Prof. J. D. Ayala - 3 -
1o
) [Ag(CN)2]-
⇒ Linear e Diamagnético
4d 5s 5p
Ag+
⇒ [Kr]4d10
⇒ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ___ ___ ___ ___
4d sp 5p
[Ag(CN)2]-
⇒ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ___ ___
2o
) [NiCl4]2-
⇒ Tetraédrico e Paramagnético
3d 4s 4p
Ni2+
⇒ [Ar]3d8
⇒ ↑↓ ↑↓ ↑↓ ↑ ↑ ___ ___ ___ ___
3d sp3
[NiCl4]2-
⇒ ↑↓ ↑↓ ↑↓ ↑ ↑ ↑↓ ↑↓ ↑↓ ↑↓
3o
) [Ni(CN)4]2-
⇒ Quadrado Planar e Diamagnético
3d 4s 4p
Ni2+
⇒ [Ar]3d8
⇒ ↑↓ ↑↓ ↑↓ ↑ ↑ ___ ___ ___ ___
Ni2+
no estado excitado:
Ni2+
⇒ [Ar]3d8
⇒ ↑↓ ↑↓ ↑↓ ↑↓ ___ ___ ___ ___
3d dsp2
4p
[Ni(CN)4]2-
⇒ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ___
4o
) [Co(NH3)6]3+
⇒ Octaédrico e Diamagnético (Complexo orbital interno – spin baixo)
3d 4s 4p
Co3+
⇒ [Ar]3d6
⇒ ↑↓ ↑ ↑ ↑ ↑ ___ ___ ___ ___
Co3+
no estado excitado:
Co3+
⇒ [Ar]3d6
⇒ ↑↓ ↑↓ ↑↓ ___ ___ ___ ___
3d d2
sp3
[Co(NH3)6]3+
⇒ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓
5o
) [CoF6]3-
⇒ Octaédrico e Paramagnético (Complexo orbital externo – spin alto)
3d 4s 4p 4d
Co3+
⇒ [Ar]3d6
⇒ ↑↓ ↑ ↑ ↑ ↑ ___ ___ ___ ___ ___ ___ ___ ___ ___
Co3+
no estado excitado:
Co3+
⇒ [Ar]3d6
⇒ ↑↓ ↑ ↑ ↑ ↑ ___ ___ ___ ___ ___ ___ ___ ___ ___
3d sp3
d2
4d
[CoF6]3+
⇒ ↑↓ ↑ ↑ ↑ ↑ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ___ ___ ___
6o
) [Co(NO2)6]4-
⇒ Octaédrico e Paramagnético em 1 e-
3d 4s 4p 4d
Co2+
⇒ [Ar]3d7
⇒ ↑↓ ↑↓ ↑ ↑ ↑ ___ ___ ___ ___ ___ ___ ___ ___ ___
Co3+
no estado excitado:
Co2+
⇒ [Ar]3d7
⇒ ↑↓ ↑↓ ↑↓ ___ ___ ___ ___ ↑ ___ ___ ___ ___
3d d2
sp3
4d
[Co(NO2)6]4-
⇒ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑ ___ ___ ___ ___](https://image.slidesharecdn.com/livro-ligaoqumicadecomplexos-151123151427-lva1-app6891/85/Livro-ligacao-quimica-de-complexos-3-320.jpg)

![Ligação Química nos Complexos - Prof. J. D. Ayala - 5 -
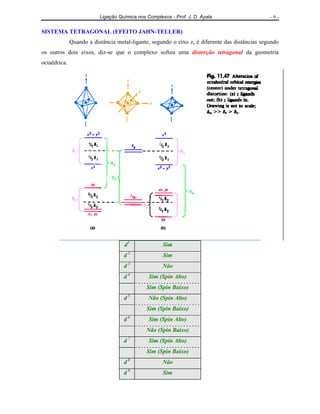
A diferença de energia entre os orbitais eg e t2g, qualquer que seja seu valor em termos
de kJ mol-1
, é definida como 10 Dq ou ∆o e denomina-se desdobramento do campo cristalino.
O valor numérico da energia que corresponde a 10 Dq é uma medida da força do campo
eletrostático. Este valor pode ser determinado a partir de dados espectrais.
ENERGIA DE ESTABILIZAÇÃO DO CAMPO CRISTALINO (EECC)
Considerando o caso mais simples de um complexo com configuração d1
, [Ti(H2O)6]3+
,
a energia necessária para promover o elétron do estado fundamental para o estado excitado,
10
2
01
2 gggg etet → , é por definição 10 Dq, seu valor pode ser obtido através do espectro de absorção
na região do UV-VIS do composto. O espectro de absorção desta amostra revela que a transição
ocorre em um máximo de 20300 cm-1
, o qual corresponde a 243 kJ mol-1
, portanto:
1-
1-
O
molkJ97,2-EECC
molkJ243)
5
2
(-.(1)EECC
)
5
2
(-.(1)EECC
=
=
∆=](https://image.slidesharecdn.com/livro-ligaoqumicadecomplexos-151123151427-lva1-app6891/85/Livro-ligacao-quimica-de-complexos-5-320.jpg)

![Ligação Química nos Complexos - Prof. J. D. Ayala - 7 -
Efeito do Campo Cristalino para um Campo Octaédrico Fraco e Forte
Campo Fraco Campo Forte
dn
Configuração
No. Elétrons
Desemparelhados
EECC Configuração
No. Elétrons
Desemparelhados
EECC
d1 1
2gt 1 0,4 ∆O
1
2gt 1 0,4 ∆O
d 2 2
2gt 2 0,8 ∆O
2
2gt 2 0,8 ∆O
d 3 3
2gt 3 1,2 ∆O
3
2gt 3 1,2 ∆O
d 4 1
ge3
2gt 4 0,6 ∆O
4
2gt 2 1,6 ∆O
d 5 2
ge3
2gt 5 0,0 ∆O
5
2gt 1 2,0 ∆O
d 6 2
ge4
2gt 4 0,4 ∆O
6
2gt 0 2,4 ∆O
d 7 2
ge5
2gt 3 0,8 ∆O
1
ge6
2gt 1 1,8 ∆O
d 8 2
ge6
2gt 2 1,2 ∆O
2
ge6
2gt 2 1,2 ∆O
d 9 3
ge6
2gt 1 0,6 ∆O
3
ge6
2gt 1 0,6 ∆O
d10 4
ge6
2gt 0 0,0 ∆O
4
ge6
2gt 0 0,0 ∆O
Energia de Emparelhamento para Alguns Íons Metálicos
Íon P [ kJ mol-1
(cm-1
) ]
Cr2+
244,3 (20425)
.d4
Mn3+
301,6 (25215)
Cr+
211,6 (17687)
Mn2+
285,0 (23825).d5
Fe3+
357,4 (29875)
Mn+
174,2 (14563)
Fe2+
229,1 (19150).d6
Co3+
282,6 (23625)
Fe+
211,5 (17680)
.d7
Co2+
250,0 (20800)](https://image.slidesharecdn.com/livro-ligaoqumicadecomplexos-151123151427-lva1-app6891/85/Livro-ligacao-quimica-de-complexos-7-320.jpg)