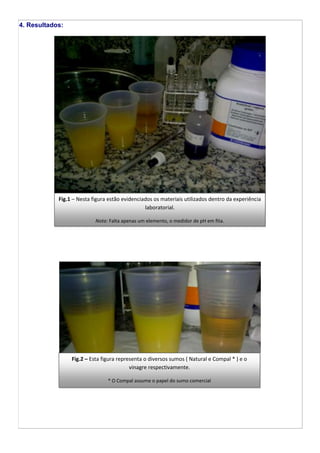
O documento descreve um experimento sobre a acidez de alimentos. Os estudantes mediram o pH de sumos naturais, sumo industrial, vinagre e bicarbonato de sódio, encontrando que o vinagre era o mais ácido e o bicarbonato a base. Eles concluíram que o pH é importante para as funções biológicas e a digestão requer diferentes níveis de acidez.