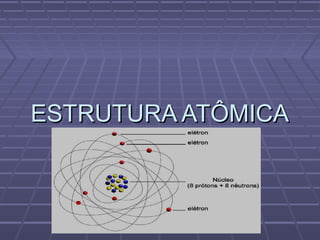
Estrutura Atômica: da Antiguidade aos Modelos Atuais
- 2. DEMÓCRITO – filósofo gregoDEMÓCRITO – filósofo grego MenorMenor partícula dapartícula da matéria.matéria. Indivisível,Indivisível, indestrutível,indestrutível, maciço,maciço, homogêneo.homogêneo.
- 3. JOHN DALTONJOHN DALTON 1776 – 18441776 – 1844 Químico e físicoQuímico e físico inglês, fundador dainglês, fundador da Teoria AtômicaTeoria Atômica ModernaModerna Célebre cientista eCélebre cientista e investigador e deinvestigador e de inteligênciainteligência invejávelinvejável..
- 4. TEORIA ATÔMICA DETEORIA ATÔMICA DE DALTONDALTON Átomos são partículas reais,Átomos são partículas reais, indivisíveis, maçicas,indivisíveis, maçicas, indestrutíveis eindestrutíveis e descontínuas de matériadescontínuas de matéria..
- 5. Os átomos de um mesmoOs átomos de um mesmo elemento são iguais e deelemento são iguais e de peso invariávelpeso invariável
- 6. Os átomos de elementosOs átomos de elementos diferentes são diferentesdiferentes são diferentes entre sientre si
- 7. Nas reações químicas, os átomosNas reações químicas, os átomos entram em proporções numéricasentram em proporções numéricas fixas, constantes, definidas.fixas, constantes, definidas. Ex: 2 Mg + OEx: 2 Mg + O22 2 MgO2 MgO
- 8. A soma das massas dosA soma das massas dos reagentes é igual a soma dasreagentes é igual a soma das massas dos produtos.massas dos produtos. Ex: 2 Mg + O2 → 2 MgOEx: 2 Mg + O2 → 2 MgO 10 g 5g 15 g10 g 5g 15 g
- 9. Retomando a idéiaRetomando a idéia de Demócrito ede Demócrito e propondo uma teoriapropondo uma teoria atômica para explicaratômica para explicar a composição daa composição da matéria, criou assimmatéria, criou assim o primeiro modeloo primeiro modelo científico, apelidadocientífico, apelidado dede Bola de Bilhar ouBola de Bilhar ou de Gude.de Gude.
- 10. TALES DE MILETOTALES DE MILETO A teoria atômica deA teoria atômica de Dalton não explicavaDalton não explicava a existência dea existência de cargas elétricas.cargas elétricas. Atritando a caneta noAtritando a caneta no cabelo ecabelo e aproximando-a deaproximando-a de pedaços de papéispedaços de papéis picados, percebeu apicados, percebeu a existência dasexistência das mesmas.mesmas.
- 11. BENJAMIN FRANKLINBENJAMIN FRANKLIN Concluiu queConcluiu que cargascargas elétricaselétricas (positivas e(positivas e negativas)negativas) fazem parte dofazem parte do átomo.átomo.
- 12. SIR JOSEPH JOHN THOMSONSIR JOSEPH JOHN THOMSON 1856 – 19401856 – 1940 Físico inglêsFísico inglês Professor daProfessor da Universidade deUniversidade de Cambridge, naCambridge, na InglaterraInglaterra Descobridor doDescobridor do elétronelétron
- 13. Descobridor do elétronDescobridor do elétron (carga elétrica negativa).(carga elétrica negativa). Esfera de carga positivaEsfera de carga positiva e elétrons incrustados eme elétrons incrustados em sua superfície.sua superfície. Modelo “Modelo “PUDIM DEPUDIM DE PASSAS”.PASSAS”. Carga total do átomo éCarga total do átomo é nula.nula. Positiva = negativaPositiva = negativa (matéria neutra).(matéria neutra).
- 14. ERNEST RUTHERFORDERNEST RUTHERFORD 1871 – 19371871 – 1937 Nascido na NovaNascido na Nova Zelândia eZelândia e radicado naradicado na Inglaterra.Inglaterra. Descobridor doDescobridor do prótonpróton
- 15. Descobridor doDescobridor do próton (cargapróton (carga positiva).positiva). Bombardeou umaBombardeou uma finíssima lâmina definíssima lâmina de ouro comouro com partículas emitidaspartículas emitidas por materialpor material radioativoradioativo..
- 16. OBSERVAÇÕES EOBSERVAÇÕES E CONCLUSÕES DECONCLUSÕES DE RUTHERFORDRUTHERFORD
- 17. 1 – OBSERVAÇÃO1 – OBSERVAÇÃO A maior parte das partículasA maior parte das partículas alfa atravessava a lâminaalfa atravessava a lâmina sem sofrer desvios.sem sofrer desvios.
- 18. 1 – CONCLUSÃO1 – CONCLUSÃO A maior parte do átomoA maior parte do átomo deve ser vazio. Nessedeve ser vazio. Nesse espaçoespaço (eletrosfera)devem estar(eletrosfera)devem estar localizados os elétrons.localizados os elétrons.
- 19. 2 – OBSERVAÇÃO2 – OBSERVAÇÃO Poucas partículas alfa (1Poucas partículas alfa (1 em 20 000) nãoem 20 000) não atravessavam a lâmina eatravessavam a lâmina e voltavam.voltavam.
- 20. 2 - CONCLUSÃO2 - CONCLUSÃO Deve existir no átomo umaDeve existir no átomo uma pequena região onde estápequena região onde está concentrada sua massa (oconcentrada sua massa (o núcleo).núcleo).
- 21. 3 - OBSERVAÇÃO3 - OBSERVAÇÃO Algumas partículas alfaAlgumas partículas alfa sofriam desvios de trajetóriasofriam desvios de trajetória ao atravessar a lâmina.ao atravessar a lâmina.
- 22. 3 – CONCLUSÃO3 – CONCLUSÃO O núcleo do átomo deveO núcleo do átomo deve ser positivo, o que provocaser positivo, o que provoca uma repulsão nas partículasuma repulsão nas partículas alfa (positivas).alfa (positivas).
- 23. OUTRAS DEDUÇÕESOUTRAS DEDUÇÕES O raio de átomo é de 10.000 aO raio de átomo é de 10.000 a 100.000 vezes maior que o raio do100.000 vezes maior que o raio do núcleo.núcleo. Propôs um modelo semelhante aoPropôs um modelo semelhante ao sistema solar.sistema solar. O núcleo do átomo (prótons) éO núcleo do átomo (prótons) é aproximadamente 1836 vezes maisaproximadamente 1836 vezes mais pesado que a eletrosfera (elétrons).pesado que a eletrosfera (elétrons).
- 24. JAMES CHADWICKJAMES CHADWICK Durante experiênciasDurante experiências com materialcom material radioativo, descobriuradioativo, descobriu os nêutrons.os nêutrons. Sem carga elétricaSem carga elétrica Localizados noLocalizados no núcleo do átomonúcleo do átomo Tem massa muitoTem massa muito próxima a dospróxima a dos prótons.prótons.
- 25. MODELO ATÔMICO ATUAL OUMODELO ATÔMICO ATUAL OU CLÁSSICOCLÁSSICO
- 26. OS NOVOS MODELOSOS NOVOS MODELOS ATÔMICOSATÔMICOS Depois de Rutherford ter propostoDepois de Rutherford ter proposto seu modelo, os cientistasseu modelo, os cientistas direcionaram seus estudos para adirecionaram seus estudos para a eletrosfera do átomo.eletrosfera do átomo.
- 27. NIELS BOHRNIELS BOHR 1885 – 19621885 – 1962 FísicoFísico dinamarquêsdinamarquês Vencedor doVencedor do prêmio Nobel deprêmio Nobel de química em 1922.química em 1922. Estudou aEstudou a eletrosfera doeletrosfera do átomo.átomo.
- 28. Os químicos jáOs químicos já sabiam quesabiam que diferentesdiferentes elementoselementos químicos emquímicos em chamachama produziam coresproduziam cores diferentes.diferentes. Modelo de BohrModelo de Bohr está relacionadoestá relacionado a distribuiçãoa distribuição dos elétrons nados elétrons na eletrosfera comeletrosfera com sua quantidadesua quantidade de energia.de energia.
- 29. IDÉIAS CENTRAIS DA TEORIAIDÉIAS CENTRAIS DA TEORIA DE BOHRDE BOHR Os elétrons giram ao redor doOs elétrons giram ao redor do núcleo em determinadasnúcleo em determinadas órbitas que apresentamórbitas que apresentam energias fixas.energias fixas.
- 30. A energia do elétrons aumentaA energia do elétrons aumenta à medida que ele se afasta doà medida que ele se afasta do núcleo, isto é, a energia danúcleo, isto é, a energia da órbita é tanto maior quantoórbita é tanto maior quanto maior for seu raio.maior for seu raio.
- 31. Os elétrons não perdem nemOs elétrons não perdem nem ganham energia, ou seja, têmganham energia, ou seja, têm energia estacionária, desdeenergia estacionária, desde que não mudem de órbita.que não mudem de órbita.
- 32. Quando se fornece energia aoQuando se fornece energia ao átomo, seus elétronsátomo, seus elétrons absorvem essa energia,absorvem essa energia, saltando de órbitas maissaltando de órbitas mais próximas para órbitas maispróximas para órbitas mais afastadas do núcleo.afastadas do núcleo.
- 33. Quando voltam a seu estadoQuando voltam a seu estado normal de energia (estadonormal de energia (estado fundamental), o átomo cede afundamental), o átomo cede a energia recebida sob a forma deenergia recebida sob a forma de ondas eletromagnéticas (luz). Aondas eletromagnéticas (luz). A energia é cedida quando seusenergia é cedida quando seus elétrons saltam para a órbita deelétrons saltam para a órbita de origem.origem.
- 35. Átomos diferentes apresentarão seusÁtomos diferentes apresentarão seus elétrons organizados de modoselétrons organizados de modos diferentes, portanto os saltos dosdiferentes, portanto os saltos dos elétrons serão variados, emitindoelétrons serão variados, emitindo ondas eletromagnéticas deondas eletromagnéticas de freqüências distintas. É por isso quefreqüências distintas. É por isso que os cientistas sabem que existe Hélioos cientistas sabem que existe Hélio no sol.no sol.
- 36. Bohr – os níveis de energiaBohr – os níveis de energia
- 37. LaserLaser Descoberto durante pesquisas deDescoberto durante pesquisas de dispositivos especiais paradispositivos especiais para excitação de elétrons em cristaisexcitação de elétrons em cristais ou gases.ou gases. Do inglês: Amplificação da luz porDo inglês: Amplificação da luz por emissão estimulada de radiação.emissão estimulada de radiação.
- 40. Um certo número de elétronsUm certo número de elétrons é estimulado a subir paraé estimulado a subir para órbitas superiores;órbitas superiores;
- 41. Quando retornam, emitem luzQuando retornam, emitem luz numa mesma freqüência, que énuma mesma freqüência, que é seguidamente refletida nosseguidamente refletida nos espelhos de cristal do aparelhoespelhos de cristal do aparelho
- 42. Isso faz crescer a intensidade e aIsso faz crescer a intensidade e a energia da luz que não seenergia da luz que não se dispersa e pode ser direcionadadispersa e pode ser direcionada com precisão na forma de feixescom precisão na forma de feixes finíssimos de alta potência.finíssimos de alta potência.
- 43. O modelo padrão do átomoO modelo padrão do átomo Física Nuclear e Química QuânticaFísica Nuclear e Química Quântica Foto cedida pelo Fermilab O modelo padrão do átomo
- 44. PARTÍCULASPARTÍCULAS 1 -1 - LéptonLépton (Elétron, Elétron-(Elétron, Elétron- Neutrino, Múon, múon-Neutrino, Múon, múon- neutrino, Tau e Tau-neutrino);neutrino, Tau e Tau-neutrino); 2 - Quarks (Up, Down, Charm, Strange,2 - Quarks (Up, Down, Charm, Strange, Top e Bottom);Top e Bottom); 3 - Bósons (Fótons, Glúons, Bósons3 - Bósons (Fótons, Glúons, Bósons vetoriais mediadores e grávitons),vetoriais mediadores e grávitons),
- 45. Podemos dizer que para cada uma delas,Podemos dizer que para cada uma delas, existe uma antipartícula, com massa igualexiste uma antipartícula, com massa igual porém com carga elétrica e momentoporém com carga elétrica e momento magnético inverso.magnético inverso. Elas dão origem ao antielétron (chamadoElas dão origem ao antielétron (chamado também de pósitron), ao antipróton e aotambém de pósitron), ao antipróton e ao antinêutron - a antimatéria, portanto.antinêutron - a antimatéria, portanto.
- 46. Matéria e antimatéria não coexistem.Matéria e antimatéria não coexistem. Quando se encontram, geram umaQuando se encontram, geram uma explosão que transforma massa emexplosão que transforma massa em energia.energia. A ciência acredita que ambas existiamA ciência acredita que ambas existiam em quantidades iguais quando ocorreu oem quantidades iguais quando ocorreu o Big Bang, mas se destruíram.Big Bang, mas se destruíram. Por alguma razão, sobrou mais matéria -Por alguma razão, sobrou mais matéria - que se moldou e formou planetas,que se moldou e formou planetas, galáxias e estrelasgaláxias e estrelas
- 47. UltrapowerUltrapower A explosão causada pelo encontro daA explosão causada pelo encontro da matéria e da antimatéria gera energia emmatéria e da antimatéria gera energia em forma de raio gama - que possui 10 milforma de raio gama - que possui 10 mil vezes mais energia que o raio solar e ovezes mais energia que o raio solar e o raio X.raio X. Só para ter uma ideia, 1 g de antimatériaSó para ter uma ideia, 1 g de antimatéria seria capaz de abastecer a cidade de Sãoseria capaz de abastecer a cidade de São Paulo durante 24 horas ou mover umPaulo durante 24 horas ou mover um carro por 10 mil km.carro por 10 mil km.
- 48. Cientistas já criaram antimatéria noCientistas já criaram antimatéria no acelerador de partículas LHC (sigla emacelerador de partículas LHC (sigla em inglês para Grande Colisor de Hádrons).inglês para Grande Colisor de Hádrons). Num túnel circular de 27 km deNum túnel circular de 27 km de comprimento, entre França e Suíça,comprimento, entre França e Suíça, átomos são manipulados para atingir aátomos são manipulados para atingir a velocidade da luz.velocidade da luz.
- 49. Ao se chocar, eles se dividem emAo se chocar, eles se dividem em partículas e antipartículas. Nessepartículas e antipartículas. Nesse processo, foi produzido um trilionésimo deprocesso, foi produzido um trilionésimo de grama de antimatéria - que daria paragrama de antimatéria - que daria para acender uma lâmpada por três segundos.acender uma lâmpada por três segundos. A antimatéria criada no LHC durou cercaA antimatéria criada no LHC durou cerca de 16 centésimos de segundo antes de sede 16 centésimos de segundo antes de se aniquilar com a matéria.aniquilar com a matéria.
- 50. UtilizaçãoUtilização A antimatéria já é utilizada em examesA antimatéria já é utilizada em exames médicos. Um exemplo é o PET Scan -médicos. Um exemplo é o PET Scan - Pósitron Emission Tomography -, quePósitron Emission Tomography -, que utiliza antielétrons para detectar tumoresutiliza antielétrons para detectar tumores cancerígenos.cancerígenos. No futuro, acredita-se que será possívelNo futuro, acredita-se que será possível desenvolver motores movidos pordesenvolver motores movidos por antimatéria - uma promissora fonte deantimatéria - uma promissora fonte de energia ilimitada.energia ilimitada.
